服務(wù)熱線
177-5061-9273

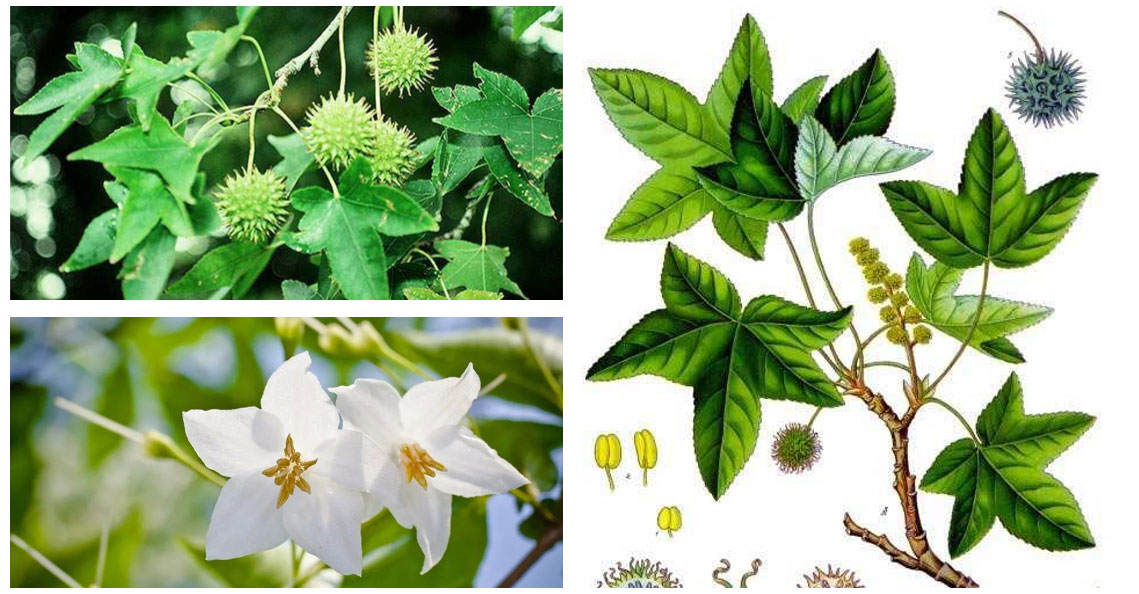
蘇合香為金縷梅科植物蘇合香樹,所分泌的樹脂(因為產(chǎn)地得名,《本草綱目》說:“此香出蘇合國,因以名之”)。蘇合國,即古代伊朗。
蘇合香是從蘇合香樹的樹脂中提取的芳香樹脂,通常在初夏的時候?qū)淦魝蚋钇粕钸_木部,使得香樹脂滲入樹皮內(nèi),秋天,剝下樹皮,榨取香樹脂,殘渣加水煮后再壓榨,榨出的香脂則是蘇合香。

再將其溶解在酒精里,過濾后,蒸去酒精,則制作成了精制蘇合香。蘇合香樹在中國不產(chǎn),李時珍說這種香產(chǎn)自蘇合香國,所以稱為蘇合香,蘇合香多產(chǎn)自非洲和西亞,但這味藥在中國被廣泛使用。蘇合香又名帝膏,是半流質(zhì)的粘稠液體,棕黃色或者暗棕色,半透明,且不溶于水。有特異的芳香氣味,味淡,微辛,以質(zhì)粘稠、含油量足、半透明、氣香濃者為佳。

化學(xué)成分
樹脂含齊墩果酮酸和3-表-齊墩果酸。綠色果實含油0.26%。
蘇合香樹脂含揮發(fā)油,內(nèi)有a-及β-蒎烯(pinene),月桂烯(myrcene),樟烯(camphene),檸檬烯(limonene),1,8-桉葉素(1,8-cineole),對聚傘花素(p-cymene),異松油烯(terpinolene),芳樟醇(linalool),松油-4-醇(4-terpineol),a-松油醇(a-terpineol),桂皮醛(cinnamicaldehyde),反式桂皮酸甲酯(trans-methylcinnamate),乙基苯酚(ethyphenol),烯丙基苯酚(allylphenol),桂皮酸正丙酯(n-propyl cinnamate),β-苯丙酸(β-phenylpropionic acid),1-苯甲酰基-3-苯基丙炔(l-benzoyl-3-phenylpropyne),苯甲酸(benzoic acid),棕櫚酸(palmitic acid),亞油酸(linoleic acid),二氯香豆酮(dihydrocoumarone),桂皮酸環(huán)氧桂皮醉酯(epoxycinnamylcinnamate),順式桂皮酸(cis-cinnamicacid),順式桂皮酸桂皮醉酯(cis-cinnamyl cinnamate)等。又含齊墩果酮酸(oleanonic acid), 3-表齊墩果酸(3-epioleanolicacid)。
藥理作用
1、抗血小板聚集功能:實驗證明蘇合香有抗血栓的作用,用蘇合香每10mg用0.1ml乙醇溶解再加1%CMC-Na0.9ml配制成混懸液,對照組為不含藥的乙醇和CMC-Na的混合液。健康家兔(體重1.9±0.4kg),雌雄兼用作試驗,結(jié)果如下:
對體外血栓形成的影響:兔耳中央動脈采血1.8ml與藥液或?qū)φ找?.2ml混勻,注入聚乙烯管環(huán)內(nèi),啟動旋轉(zhuǎn)環(huán)使血液在37℃環(huán)境中以17/r/min轉(zhuǎn)動15分鐘。自環(huán)內(nèi)傾出血栓,立即量取血栓長度和濕重,然后將血栓置20℃恒溫器烘干20分鐘,稱取血栓干重。結(jié)果對照組:血栓長度7.6±2.3cm,血栓濕重202.4±48.1mg,血栓干重105.6±21.4mg;蘇合香組:血栓長度3.7±0.4cm,血栓濕重116.2±20.7cm,血栓干重55.7±14.1mg。與對照組比較,蘇合香lmg/ml,顯著抑制體外血栓形成。
對血小板內(nèi)cAMP含量的影響:測定血小板內(nèi)cAMP含量。結(jié)果對照組7.4±2.8pmol/mg蛋白,蘇合香大劑量2mg/ml為14.7±4.1pmol/mg蛋白,小劑量1mg/ml為7.5±3.1pmol/mg蛋白。與對照組比較,蘇合香大劑量組可顯著提高血小板內(nèi)cAMP含量(P<0.001)。
對凝血功能的影響:
(1)體外實驗:測定復(fù)鈣時間和凝血酶原時間,白陶土部分凝血活酶時間和纖溶酶活性。蘇合香能明顯延長血漿復(fù)鈣時間、凝血酶原時間和白陶土凝血活酶時間、顯著提高纖溶酶活性。
(2)體內(nèi)實驗:家兔灌胃給藥蘇合香100mg/kg,容積為10ml,對照組給予等容積乙醇和CMC-Na的混合液,同時給生理鹽水作空白對照。按照給藥前、給藥后不同時間取血樣作下述各項測定。結(jié)果表明蘇合香口服給藥能明顯延長復(fù)鈣時間,凝血酶原時間和白陶土部分凝血活酶時間,降低血漿纖維蛋白含量,促進纖溶酶活性。蘇合香抗血小板聚集的主要成分是順式桂皮酸。
2、對心血管的影響:冠心蘇合丸可使實驗性心肌梗塞犬的冠竇血流量明顯增加,使其恢復(fù)正常或接近正常,并能明顯減慢心率,降低心肌耗氧量;對于非心肌梗塞大的冠竇血流量無明顯影響,但可減慢心率,降低心肌耗氧量。拆方研究表明冠心蘇合丸組成中藥中僅蘇合香及冰片具有上述作用,另外幾味藥無效。由蘇合香與冰片兩藥組成的蘇冰滴丸具有顯著的抗心肌缺血的效果,對于游泳應(yīng)激及垂體后葉素所致小鼠心肌缺血性超威結(jié)構(gòu)改變有明顯的保護效果,并能對抗垂體后葉素所致心肌營養(yǎng)性血溶量的降低,對抗去甲腎上腺素所致的主動脈收縮。
3、抑菌、抗炎作用:蘇合香有較弱的抗菌作用,可用于各種呼吸道感染。蘇合香還有溫和的刺激作用,用于局部可緩解炎癥,如濕疹和瘙癢,并能促進潰瘍與創(chuàng)傷的愈合。
蘇合香的藥用功效
1、寒閉神昏:蘇合香氣辛香而性溫,有較好的開竅醒神之效,又可溫里散寒、化解濕濁,故宜于中風(fēng)、癇證等屬寒邪、痰濁閉阻心竅所致之神昏。并常與開竅醒神,溫里散寒之品配伍,如《外臺秘要》蘇合香丸,以之與麝香、沉香、檀香等同用。
2、胸腹冷痛:蘇合香具有溫里散寒、止痛的功效,宜于寒凝氣滯所致疼痛。治胸腹脹滿冷痛,胸痹痛,常與溫里散寒、行氣止痛之品同用,如《外臺秘要》蘇合香丸及其衍化方亦可主治以上病證。
蘇合香在香譜及典籍上的記載
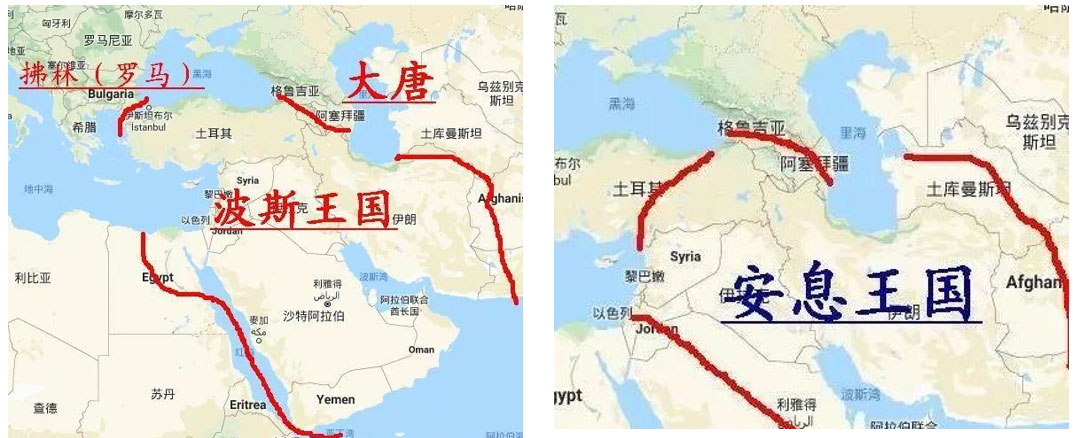
蘇合香和安息香、乳香一樣都是來自西域的樹脂類香料,質(zhì)地堅實,芳香異常。大秦國人采到蘇合香之后,將其煎出汁水,用以凝結(jié)成香膏,并將煎剩的渣滓賣給各國商人。所以,輾轉(zhuǎn)販賣到中國的蘇合香香氣不濃。《新修本草》謂:“此香從西域及昆侖來。”《唐本草》:蘇合香為紫赤色,與紫檀香類似,質(zhì)地像石頭一樣堅實,芳香異常。焚燒后變成灰白色的為佳品。[時珍說]此香出自蘇合國,因此得名。[恭說]來自西域及昆侖。紫赤色,與紫檀相似,堅實,極香。[頌說]廣州雖然也有蘇合香,但與蘇木類似,無甚香氣。藥中只用氣味極濃烈者。[時珍說]蘇合香出于安南、三佛齊諸國。樹生膏,可為藥,以氣味濃烈而無渣滓者為上。沈括《夢溪筆談》載,蘇合香赤色如堅木,又有蘇合油如明膠,人多用它。
主辟惡,溫瘧,癇座。去濁,除邪,令人無夢魘。——《名醫(yī)別錄》
殺蟲毒。療癲癇,止氣逆疼痛。——《本草正》
利水消腫,治脹,疹痱,氣積血癥,調(diào)和臟腑。——《玉楸藥解》
成品選鑒
半流質(zhì)的黏稠液體,棕黃色或暗棕色,半透明,不溶于水。有特異芳香氣,昧淡,微辛。以質(zhì)黏稠、含油足、半透明、氣香濃者為佳。
實用妙方
蘇合香丸:可治結(jié)核,霍亂,鬼魅瘴瘧,赤白暴痢,瘀血月閉,疲癖疔腫,小兒驚癇客忤,大人中風(fēng),中氣,心痛等癥。用蘇合油一兩,安息香末二兩,以酒熬成膏,入蘇合油內(nèi)。白術(shù)、香附子、丁香、青木香、白檀香、沉香、麝香、蓽芨、訶梨勒(煨、去核)、朱砂、烏犀牛角各二兩,龍腦、熏陸香各一兩,研末,以香膏加煉蜜和成劑,蠟紙包收。每服旋丸如梧桐子大,早取井華水,化服四丸。老人、小孩各一丸。
水汽浮腫:蘇合香、白粉、水銀等份,搗勻,以蜜制成如小豆大的丸,每服二丸,白水送服。
北宋第三位皇帝真宗趙恒對蘇合香酒情有獨鐘,不僅自己飲用,還推薦給大臣,使飲用蘇合香酒在當(dāng)時成為一種流行。據(jù)《墨客揮犀》記載,王文正太尉氣羸多病,真宗面賜藥酒一瓶,令空腹飲之,可以和氣血,辟外邪。文正飲之,大覺安健,因?qū)ΨQ謝,上曰“此蘇合香酒也”。宋真宗認為,這種酒能“調(diào)五臟,卻腹中諸疾,每冒寒夙興,則飲一杯”。其藥用功效在《本草綱目》中得到了證實,“氣香竄,能道諸竅臟腑,故其功能辟一切不正之氣”。

1、蘇合香,一種治療心腦血管疾病的有前途的植物性藥物:綜述
近年來,心腦血管疾病的發(fā)病率和死亡率逐年上升,已成為全球性的負擔(dān)和挑戰(zhàn)。基于“腦病心”、“心病腦”的整體思維,結(jié)合中醫(yī)多靶點、多路徑效應(yīng)的特點,中醫(yī)在心腦血管疾病的治療上更有優(yōu)勢。作為一種植物醫(yī)學(xué),蘇合香因其復(fù)蘇,避免污穢和減輕疼痛的效果,在心腦血管疾病的治療。通過對近10年國內(nèi)外相關(guān)文獻的查閱和整理,對蘇合香的藥用部位、傳統(tǒng)用途和化學(xué)成分進行了綜述。第一次,基于“大腦和心臟同時治療”的理念,總結(jié)分析了蘇合香治療心腦血管疾病的藥理活性及保護心腦的機制,表明蘇合香具有抗腦缺血、調(diào)節(jié)血腦屏障、雙向調(diào)節(jié)中樞神經(jīng)系統(tǒng)的藥理作用,抗心肌缺血、抗心律失常、抗血栓形成、抗血小板聚集。主要通過抑制炎癥免疫因子、抗氧化應(yīng)激、抗凋亡、促新生血管形成、調(diào)節(jié)NO釋放等機制對腦和心臟發(fā)揮保護作用。當(dāng)前的結(jié)果和局限性的基礎(chǔ)上,未來的研究策略和觀點提出了安息香,以提供一個參考這種藥的進一步應(yīng)用和發(fā)展,以及促進新思想和臨床應(yīng)用的“同步治療腦心”。
Storax (ST)又名安息香或蘇合香,是金縷梅科蘇合香(Liquidambar orientalis Mill)樹干分泌的一種經(jīng)過加工精制的芳香樹脂。它不僅在東亞、印度、非洲和土耳其被廣泛用作民間藥,而且是一種受歡迎的食物和酒的香料。在秦漢時期,蘇合香通過絲綢之路傳入中國,并廣泛應(yīng)用于醫(yī)療保健和社會生活。由于其安全性高,對多種疾病都有良好的療效,蘇合香是制備冠心素合丸、麝香保心丸、素冰滴丸、蘇合香片等中藥方劑的關(guān)鍵成分。目前,含有蘇合香的中藥化合物在亞洲國家被廣泛用于心腦血管疾病的預(yù)防和治療。
CCVD是由血液增稠、動脈粥樣硬化、高血壓、高脂血癥等引起的心腦缺血或出血性疾病,包括心腦血管病變,對人類健康構(gòu)成嚴(yán)重威脅。根據(jù)《2016年全球疾病負擔(dān)》,全球約有8010萬人患有腦血管疾病,其中6760萬人患有缺血性中風(fēng),270萬人死亡。與缺血性中風(fēng)相似,冠心病的發(fā)病率也很高。2016年,估計有1790萬人死于心腦血管疾病,占全球死亡人數(shù)的31%。因此,為了預(yù)防和治療這些疾病,明確CCVD的發(fā)病機制,闡明心腦血管疾病之間的關(guān)系,從而找到療效更好、副作用更少的藥物是當(dāng)務(wù)之急。
中醫(yī)認為,人是一個有機整體。雖然“腦”和“心”是兩個不同的器官,但它們在病理上是相互關(guān)聯(lián)的,CCVD往往同時存在。據(jù)報道,冠心病患者中風(fēng)的發(fā)生率為兩倍以上,高血壓患者為三倍以上,心力衰竭患者為四倍,心房顫動患者為五倍。同樣,中風(fēng)(腦缺血、腦出血或蛛網(wǎng)膜下腔出血)可導(dǎo)致心功能不全、心律失常,最終導(dǎo)致心力衰竭。中風(fēng)后大腦和心臟的相互作用如圖1所示。通過調(diào)節(jié)下丘腦-垂體-腎上腺軸,激活交感神經(jīng)和副交感神經(jīng)釋放兒茶酚胺,擾亂腸道菌群,誘導(dǎo)免疫反應(yīng)和炎癥,釋放微囊泡,卒中后可誘發(fā)心功能不全。因此,采用“腦心并作”的方法學(xué)是合理的,也是必然的,靈活運用這一原則有助于提高CCVD的療效。目前已從蘇合香中分離出84個化學(xué)成分,主要包括萜類、芳香有機酸及其衍生物,具有抗凝、抗炎、抗菌等多種藥理活性。
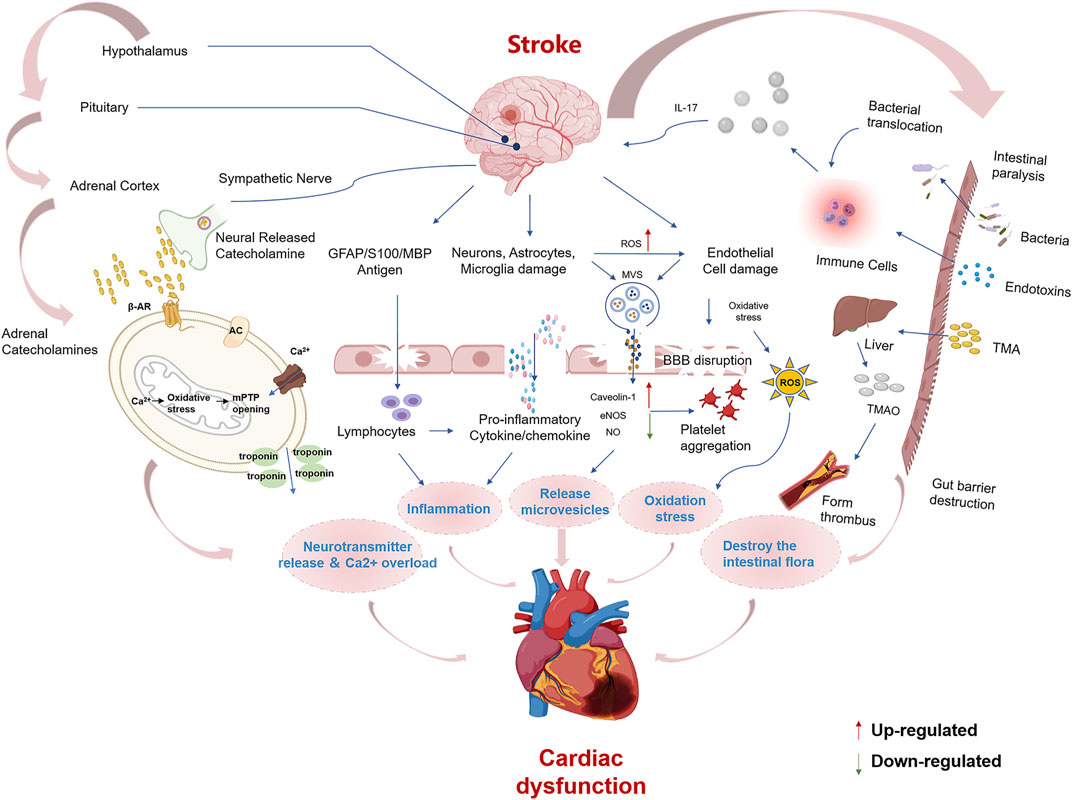
圖1 腦卒中后腦-心關(guān)聯(lián)機制概述腦卒中后心功能不全可能由以下機制引起:①下丘腦-垂體-腎上腺軸的激活和交感神經(jīng)的調(diào)節(jié)引起作用于β受體的兒茶酚胺的激增。β-受體偶聯(lián)刺激G蛋白激活腺苷酸環(huán)化酶(AC),導(dǎo)致線粒體Ca2+超載和ATP合成失敗,導(dǎo)致心肌細胞死亡。②中風(fēng)后死亡的腦細胞會釋放出破壞性的抗原,這些抗原可通過破裂的血腦屏障進入人體循環(huán),抗原特異性自身免疫反應(yīng)導(dǎo)致促炎細胞因子的分泌。受損的神經(jīng)元、小膠質(zhì)細胞、內(nèi)皮細胞和星形膠質(zhì)細胞,以及脾臟可刺激促炎細胞因子和趨化因子的釋放。③腦卒中后受損星形膠質(zhì)細胞、神經(jīng)元和小膠質(zhì)細胞釋放的微囊泡(Microvesicles, mv)抑制eNOS功能,增加Caveolin-1,降低NO合成,導(dǎo)致內(nèi)皮功能障礙和血小板聚集。④活性氧升高和內(nèi)皮細胞損傷導(dǎo)致氧化應(yīng)激。⑤中風(fēng)增加腸道屏障的通透性,引起腸道菌群失調(diào),細菌和內(nèi)毒素移位進入血液。氧化三甲胺是微生物代謝產(chǎn)物TMA的肝臟氧化產(chǎn)物。氧化三甲胺誘發(fā)血栓形成和動脈粥樣硬化的形成。
近年來,國內(nèi)外研究人員對CCVD的研究取得了許多成果。然而,目前還沒有針對ST在ccvd治療中的各個重要方面進行系統(tǒng)、全面的綜述。本文與“安息香”,“蘇合香”和“Su-Hexiang”作為關(guān)鍵詞,藥用部分,傳統(tǒng)用法,植物化學(xué),和藥理活性的蘇合香在過去10年里總結(jié)了通過搜索相關(guān)文件在CNKI,中國國家知識基礎(chǔ)設(shè)施,網(wǎng)絡(luò)科學(xué),PubMed和其他數(shù)據(jù)庫。討論了當(dāng)前工作的局限性,并對蘇合香未來的研究方向進行了展望,這對蘇合香的深入探索、開發(fā)和利用至關(guān)重要,將為CCVD的臨床診斷和治療提供新的思路。此外,還為“腦心同時調(diào)節(jié)”理論的應(yīng)用提供了依據(jù)。
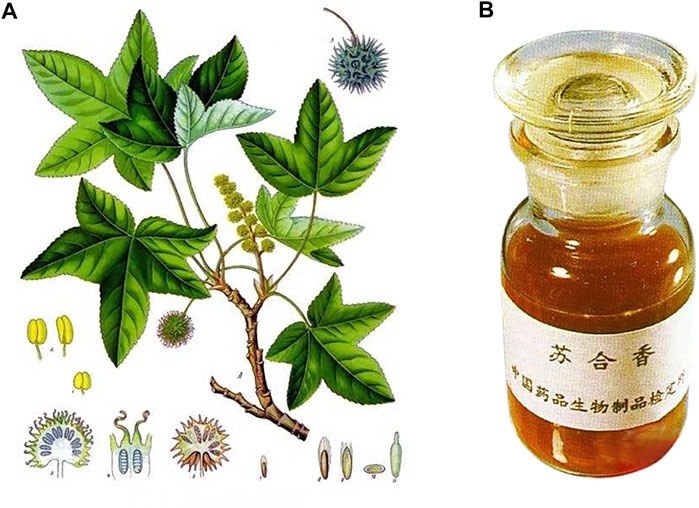
圖2 蘇合香的枝葉(A);蘇合香油 (B) (https://image.baidu.com/)
蘇合香(Liquidambar orientalis Mill.)是一棵樹,其枝葉如圖2A所示。這種植物原產(chǎn)于小亞細亞南部,特別是土耳其和敘利亞北部。目前在中國廣西省有幾種介紹。樹皮通常在初夏被敲擊或折斷,這樣樹脂就會分泌并滲透到樹皮中。秋天,將受傷的樹皮剝落,提取樹脂。剩下的殘渣在水中煮沸,再次壓榨,然后過濾出雜質(zhì),提取出香脂,就像普通的香脂一樣。香脂溶解在乙醇中,過濾后蒸出乙醇。而后成為精制香脂,又稱蘇合香油或流動蘇合香,其特征為半流體、棕色或深褐色、半透明、粘稠、芳香,如圖2B所示(國家中醫(yī)藥管理局編委,1998)。
1.1 抗腦缺血
缺血性腦損傷是一個復(fù)雜的病理生理過程,涉及NO神經(jīng)毒性、炎癥介質(zhì)刺激和釋放、鈣超載、細胞凋亡等多種因素。而蘇合香在干預(yù)腦缺血病理損傷中表現(xiàn)出多環(huán)節(jié)、多途徑作用的特點。結(jié)果表明,蘇合香顯著抑制Na2S2O4誘導(dǎo)的PC12細胞缺血缺氧損傷,抑制OGD/ R誘導(dǎo)的腦血管內(nèi)皮細胞、星形膠質(zhì)細胞和皮層神經(jīng)元細胞缺血缺氧損傷,增強細胞活力。我們還發(fā)現(xiàn)蘇合香顯著增加了小鼠斷頭后的開口數(shù)量,也延長了注射飽和氯化鎂溶液引起缺氧的小鼠的開口時間,降低MCAO大鼠腦組織病理損傷程度和腦梗死體積。這些結(jié)果表明蘇合香對缺血腦組織有明顯的改善作用,其主要作用機制如圖3所示,包括抑制Ca2+超載、改善血液流變學(xué)、抗腦細胞凋亡、抗氧化應(yīng)激、抑制炎癥介質(zhì)、促進血管生成、一氧化氮的產(chǎn)生和血腦屏障(BBB)的調(diào)節(jié)等。
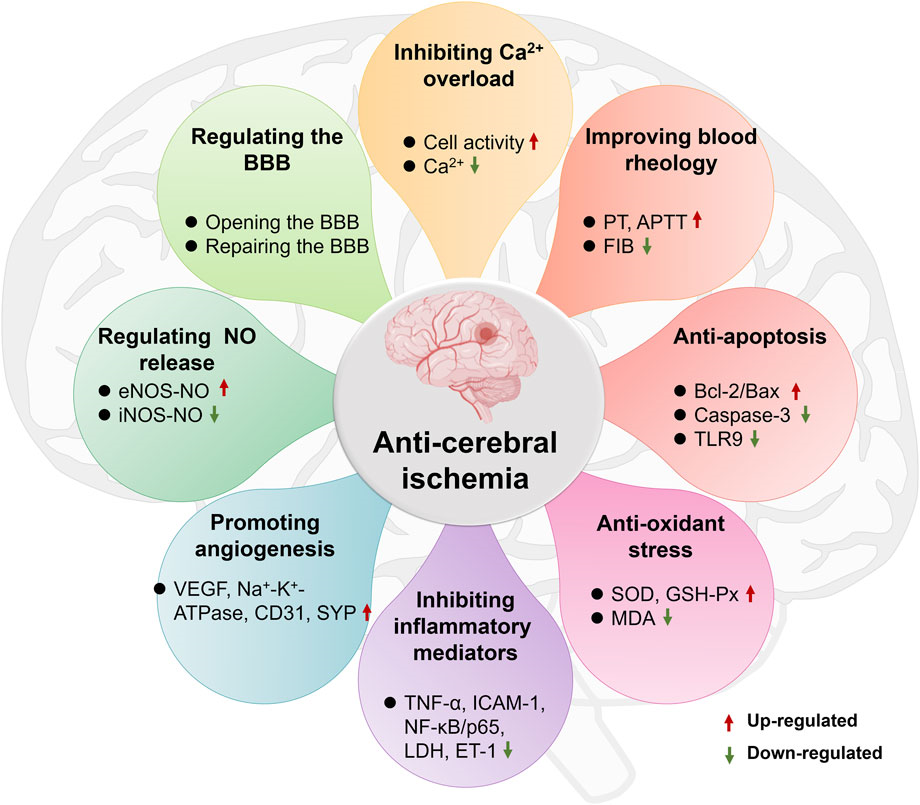
圖3 蘇合香治療腦缺血的主要藥理機制
1.2 鎮(zhèn)靜和抗驚厥藥
驚厥是由各種原因引起的中樞神經(jīng)過度興奮的癥狀。戊四唑通過阻斷中樞神經(jīng)系統(tǒng)γ -氨基丁酸(GABA)的活性誘發(fā)驚厥。研究發(fā)現(xiàn)蘇合香可顯著延長戊四唑誘導(dǎo)的驚厥潛伏期,從而降低驚厥死亡率。提示蘇合香可能通過GABA神經(jīng)調(diào)節(jié)途徑發(fā)揮抗驚厥作用。對士的寧(strychnine)和木防己苦毒素(picrotoxin)引起的驚厥也有顯著的治療作用。長期吸入蘇合香揮發(fā)油可延長戊巴比妥誘導(dǎo)的睡眠,鼻吸入比灌胃更快地具有鎮(zhèn)靜和抗驚厥作用,并顯著降低腦組織MDA和谷氨酸含量。說明蘇合香揮發(fā)油具有一定的鎮(zhèn)靜和抗氧化作用。由于興奮性氨基酸是在氧化應(yīng)激狀態(tài)下釋放的,因此認為蘇合香的抗驚厥作用也與其抗氧化作用有關(guān),這為其在治療驚厥中的臨床應(yīng)用提供了理論依據(jù)。鼻腔給藥本身可以提高藥物劑量,因為藥物通過鼻腔進入大腦有兩種途徑:一種是通過嗅覺粘膜直接進入大腦;另一種則通過呼吸區(qū)粘膜進入體循環(huán),然后通過血腦屏障進入大腦,吸收迅速,有效。因此,鼻給藥對于急性中樞系統(tǒng)疾病的治療非常重要,蘇合香自然調(diào)整血腦屏障的優(yōu)勢,結(jié)合給藥方式的優(yōu)化,對開發(fā)新型高效的中樞靶向藥物具有重要意義。
1.3 興奮中心
芳合香復(fù)蘇藥物對中樞神經(jīng)系統(tǒng)興奮性具有雙向調(diào)節(jié)作用,既具有“安神”作用,又具有“誘導(dǎo)復(fù)蘇”作用。有研究表明,口服蘇合香可增加大鼠紋狀體中天冬氨酸含量,降低甘氨酸含量,甘氨酸在神經(jīng)遞質(zhì)中起興奮作用。與以往延長戊巴比妥鈉睡眠時間的結(jié)果不同,蘇合香還可以縮短戊巴比妥鈉的睡眠時間,表現(xiàn)出大腦喚醒和興奮的作用。兩種截然相反的結(jié)果的原因可能是,長期吸入蘇合香揮發(fā)油相當(dāng)于增加劑量的藥物,具有鎮(zhèn)靜效果類似于氣體麻醉,而口服“開竅醒神”“inducing-resuscitation”效應(yīng),中扮演興奮中心的重要角色。但這一假設(shè)并未在同一整體實驗中得到證實,需要通過多個模型、多個指標(biāo)來驗證。
1.4 抗心肌缺血
心肌缺血是心臟供血、灌注減少,氧供應(yīng)減少,導(dǎo)致能量代謝異常,心臟不能正常工作的一種病理狀態(tài)。它是心肌梗死、動脈粥樣硬化等多種心血管疾病的主要發(fā)病機制。多項研究證實蘇合香對心肌缺血大鼠的心肌梗死面積和心肌梗死率有抑制作用。病理檢查表明,能改善缺血引起的心肌細胞壞死、變性、出血、水腫,提示其對缺血心肌有保護作用。由于心肌缺血的發(fā)病機制復(fù)雜多樣,蘇合香在抗心肌缺血中的主要機制見圖4,包括調(diào)節(jié)神經(jīng)遞質(zhì)、調(diào)節(jié)心肌酶譜、擴張冠狀動脈、改善血液流變學(xué)和血流動力學(xué)、抗脂質(zhì)過氧化、抗心肌細胞凋亡,抗血栓和抗血小板聚集。
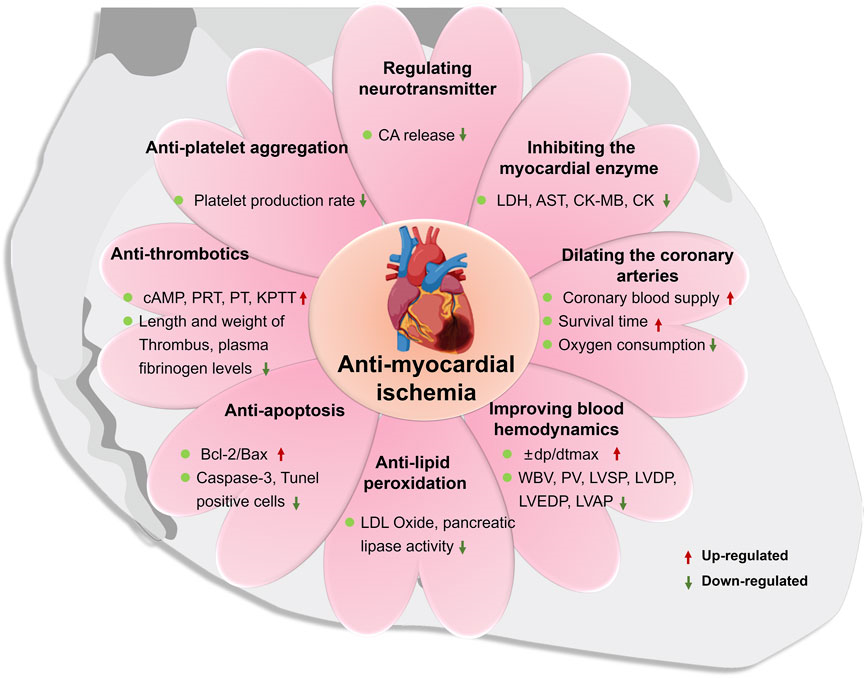
圖4 蘇合香治療心肌缺血的主要藥理機制
1.5 抗心律失常
心律失常是指心臟起搏和傳導(dǎo)功能障礙引起的心律、頻率或激活序列異常,主要表現(xiàn)為心動過速、心動過緩、心律失常、傳導(dǎo)阻滯和驟停,可導(dǎo)致暈厥、猝死等危重情況。現(xiàn)代抗心律失常藥物治療心律失常有效,但有大量不良反應(yīng),除肝、腎損害外,甚至一些抗心律失常藥物也有相同的致心律失常不良反應(yīng)。中藥抗心律失常具有良好的臨床療效和安全性。在改善臨床癥狀的同時,可提高患者的生活質(zhì)量。有研究表明蘇合香可顯著降低氯仿致小鼠心律失常的發(fā)生率,且隨著劑量的增加有增強的趨勢。Ren等人通過TI+通量篩查方法篩選出了25種被認為可以緩解心律失常的中藥。發(fā)現(xiàn)蘇合香可阻斷Kir2.1的內(nèi)外電流,是首個阻斷Kir2.1及其突變體的中藥,有望成為治療3型短QT綜合征(sqt3)的靶向藥物。進一步的研究發(fā)現(xiàn),其作用的有效成分是氫化肉桂酸,但其作用機制尚待明確。
1.6 蘇合香治療心腦血管疾病的總結(jié)與展望
蘇合香是最受歡迎的民間藥物之一,在亞洲和非洲有廣泛使用的歷史,在預(yù)防和治療心腦血管疾病(心絞痛、心肌梗死、中風(fēng)、腦動脈粥樣硬化)方面有顯著的療效。綜上所述,蘇合香可通過抗炎、抗氧化應(yīng)激、抗凋亡、促血管生成等常見藥理機制發(fā)揮腦-心保護作用,具體調(diào)控示意圖如圖5所示。然而,目前國內(nèi)外文獻對蘇合香的研究還不夠深入,一些報道已經(jīng)過時,單劑量、缺乏對照或僅進行體外研究。中藥藥理研究應(yīng)精心設(shè)計,詳細記錄給藥劑量、給藥途徑和給藥頻次,采用合適的模型和準(zhǔn)確的計量方法。無論是在體外還是在體內(nèi)都不能復(fù)制機體的復(fù)雜環(huán)境,因此還不足以準(zhǔn)確評估藥物的效果。因此,我們建議根據(jù)共識文件的要求,結(jié)合體內(nèi)和體外研究,同時研究多個劑量的藥理學(xué)研究。
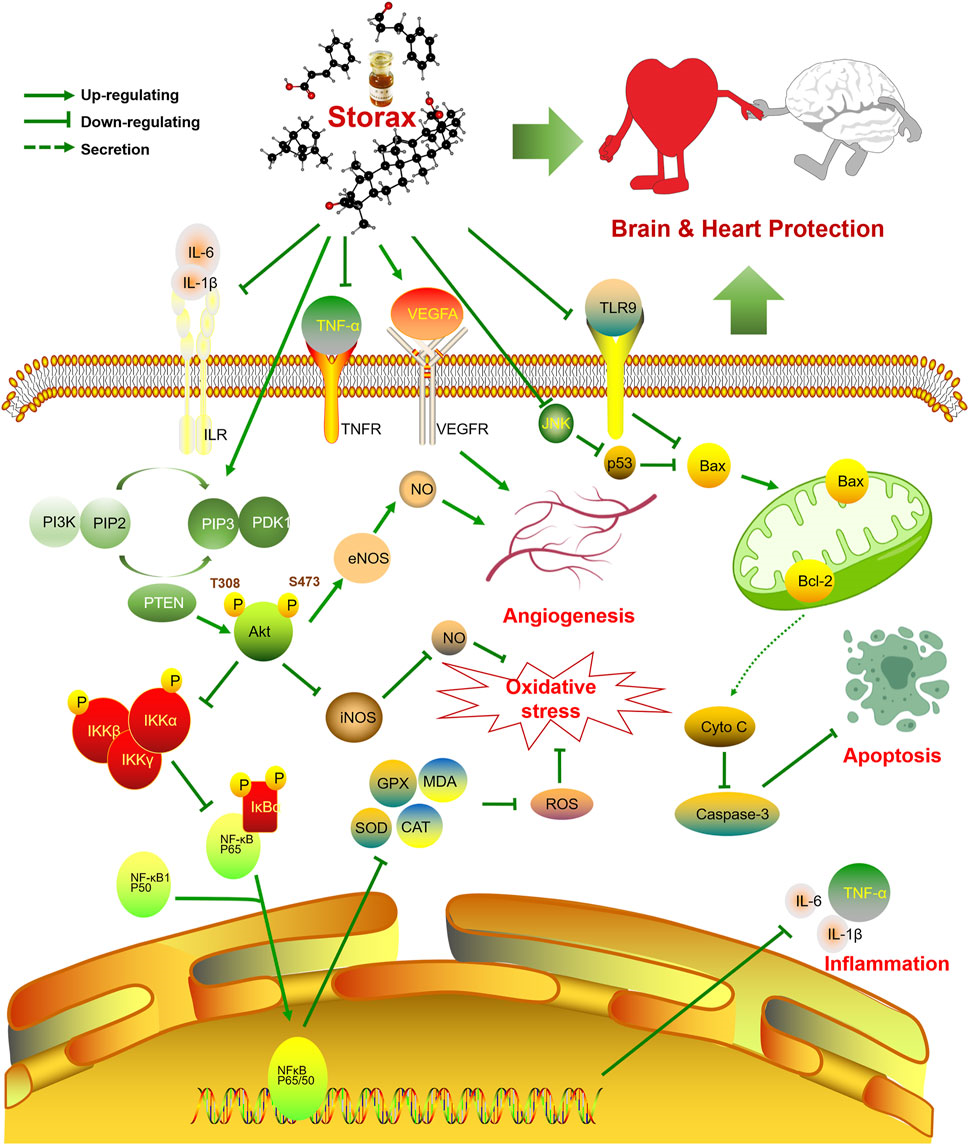
圖5 蘇合香對腦心保護作用的調(diào)節(jié)機制示意圖。蘇合香可以激活PI3K/Akt信號通路和抑制NF-κB信號通路,進而可以在調(diào)節(jié)生產(chǎn)中發(fā)揮作用,抗炎,氧化壓力和促血管生成藥理作用,以及由升降bcl-2的表達和抑制抗凋亡Caspase-3和Bax,因此在大腦和心臟中起著共同的保護作用。
①深入探討蘇合香對腦和心臟保護作用的化學(xué)成分。雖然從蘇合香中分離和鑒定出了大量的化合物,但只有少數(shù)的化合物得到了藥理上的評價。因此,深入研究蘇合香的化學(xué)成分及其藥理作用,特別是其生物活性成分的作用機制,闡明民族醫(yī)學(xué)用途與生物活性之間的關(guān)系,無疑將是進一步研究的重點。由于其效價的化學(xué)成分研究尚處于粗提階段,其特定的有效成分尚未分離鑒定,難以建立兩者之間的關(guān)系,從而影響各方面的進一步研究。因此,現(xiàn)行版《中華人民共和國藥典(2020版)》對蘇合香有明確的質(zhì)量標(biāo)準(zhǔn),但由于其特異性弱、含量限制低,仍無法有效區(qū)分贗品。在指示劑成分的識別和指紋鑒定方面的科學(xué)研究已經(jīng)取得了很大的進展。然而,還需要進一步努力將這些結(jié)果納入法律質(zhì)量標(biāo)準(zhǔn)。建立更加合理有效的評價體系,提高蘇合香的質(zhì)量,尋找具體的給藥范圍,確保臨床用藥安全有效,為蘇合香資源的開發(fā)利用提供參考依據(jù)。
②建立“腦-心”疾病模型是未來的發(fā)展方向。蘇合香對CCVDs的療效充分體現(xiàn)了中醫(yī)的原則“同時治療大腦和心臟”,但它仍然需要通過構(gòu)造一個對于心腦血管疾病的模型來驗證,以在同一時間治療和減少心臟和大腦組織的病理損害。此外,復(fù)方中蘇合香的比效價和強度尚不清楚,有效成分的處方研究較少。對心腦血管損傷后多個病理方面的干預(yù)作用進行了廣泛的橫向(cross-sectional)研究,但對個體病理方面的深入縱向研究較少,分子生物學(xué)水平的研究也較少。因此,有必要通過系統(tǒng)藥理學(xué)方法,結(jié)合多組學(xué)工具,進一步探索其生物活性和潛在的藥理機制,篩選和預(yù)測活性物質(zhì)的靶點,闡明其具體的藥理機制。
③蘇合香調(diào)節(jié)血腦屏障的穩(wěn)態(tài)機制有待進一步研究。血腦屏障的特殊功能使腦血管疾病的治療困難,因為大部分的藥物很難通過血腦屏障,使得藥物傳遞到中樞神經(jīng)系統(tǒng)和大腦中未能積累達到足夠的劑量從而影響療效。近年來,如何促進血腦屏障的有效開放,提高中樞神經(jīng)系統(tǒng)疾病的療效逐漸成為研究熱點。蘇合香一方面可以起到神經(jīng)保護作用,另一方面可以打開血腦屏障,使藥物本身及伴隨藥物進入腦實質(zhì),直接起到神經(jīng)保護作用。但令人擔(dān)憂的是,在蘇合香打開血腦屏障的同時,是否會有有害物質(zhì)隨藥物進入腦實質(zhì)(brain parenchyma),加重神經(jīng)損傷,尚待進一步研究血腦屏障打開的機制和時間窗。
④蘇合香藥效學(xué)物質(zhì)的藥代動力學(xué)過程有待探索。到目前為止,關(guān)于蘇合香的藥代動力學(xué)的報道相對較少,這部分報道仍采用高效液相色譜法建立以肉桂酸為測定指標(biāo)的藥代動力學(xué)研究。然而,由于其多組分、易揮發(fā)性,單個組分的藥代動力學(xué)參數(shù)的測定可能不能代表其他組分在體內(nèi)的實際過程。蘇合香的毒理學(xué)研究很少。蘇合香抑制人細胞色素P450酶(CYPs),這是一把雙刃劍。一方面,蘇合香與一些以CYP為基礎(chǔ)的治療窗較窄的藥物(如華法林、地高辛等)聯(lián)合使用可能會引發(fā)中草藥相互作用,抑制藥物代謝,引起臨床不良反應(yīng)或并發(fā)癥。另一方面,蘇合香可能通過阻斷CYP類藥物的代謝清除率,延長CYP類藥物的使用時間,有利于清除率相對較快的CYP類藥物的使用,從而提高治療效果。這些作用的有效成分是五環(huán)三萜類化合物。總之,蘇合香在體內(nèi)的過程需要系統(tǒng)的了解和深入的研究。對蘇合香本身血液和代謝成分的研究,以及與其他藥物的結(jié)合,將有助于更好地調(diào)節(jié)臨床使用的適應(yīng)癥和禁忌癥。
綜上所述,蘇合香對CCVD的治療效果充分體現(xiàn)了中醫(yī)“心腦兼治”的治療原則,符合整體醫(yī)學(xué)的治療策略,具有很大的發(fā)展?jié)摿脱芯績r值。今后應(yīng)在已有研究的基礎(chǔ)上,規(guī)劃進一步的深入研究,避免低水平的重復(fù),取得新的進展和突破。
2、蘇合香通過抑制NF-κB活化保護體外氧-葡萄糖剝奪/復(fù)氧誘導(dǎo)的星形膠質(zhì)細胞損傷
中風(fēng)是世界上第二大死亡原因,也是長期殘疾的主要原因。目前迫切需要開發(fā)一系列神經(jīng)保護策略,以抑制中風(fēng)后數(shù)小時和數(shù)天內(nèi)發(fā)生的損害。蘇合香是中藥蘇合香(Liquidambar orientalis Mill)中提取的天然樹脂,多年來一直用于治療急性中風(fēng)。蘇合香已證實對腦血管疾病有神經(jīng)保護作用。然而,蘇合香激活缺血/再灌注損傷星形膠質(zhì)細胞的神經(jīng)保護機制尚未闡明。本研究建立OGD/R誘導(dǎo)的星形膠質(zhì)細胞損傷模型,探討蘇合香對OGD/R誘導(dǎo)的星形膠質(zhì)細胞損傷的影響及其機制。實驗結(jié)果表明,蘇合香能減輕炎癥細胞因子的表達,保護OGD/R損傷的原代皮層星形膠質(zhì)細胞。此外,蘇合香可通過OGD/R抑制損傷星形膠質(zhì)細胞NF-κB的活化,而通過Bay-11-7082抑制NF-κB則可使蘇合香的神經(jīng)保護作用被掩蓋。綜上所述,蘇合香可減輕炎癥細胞因子的表達,保護OGD/R損傷的原代皮層星形膠質(zhì)細胞,其作用機制可能與NF-κB信號通路的激活有關(guān)。
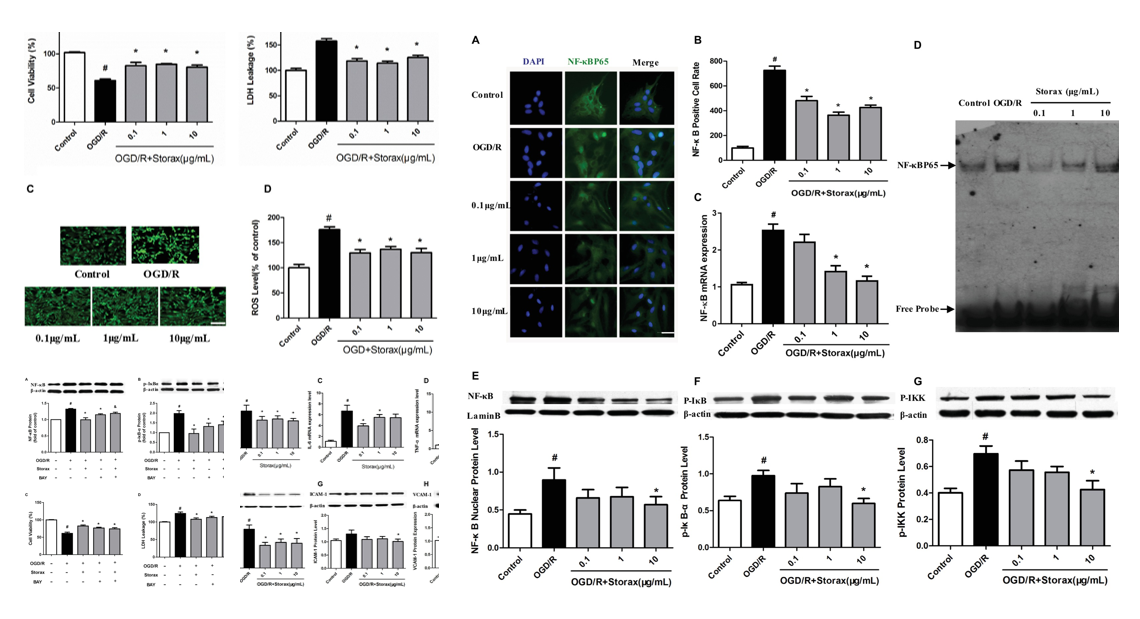
實驗結(jié)果表明,蘇合香通過降低OGD/R后受損的初級皮層星形膠質(zhì)細胞中一系列炎癥因子的表達,發(fā)揮了相當(dāng)大的神經(jīng)保護作用。這些保護作用是由NF-κB的抑制介導(dǎo)的,并且可以通過Bay-11-7082的預(yù)處理部分逆轉(zhuǎn)。
缺血性中風(fēng)引發(fā)了大腦中一系列復(fù)雜的病理生理事件,包括興奮性毒性、酸中毒、炎癥、氧化應(yīng)激、梗死周圍去極化和凋亡,尤其是炎癥和凋亡的有害影響,最終導(dǎo)致細胞死亡和梗死。上述過程相互作用,形成了腦缺血后復(fù)雜的病理形態(tài)。越來越多的證據(jù)表明,膠質(zhì)細胞特別是星形膠質(zhì)細胞在腦缺血的病理生理學(xué)中發(fā)揮重要作用。星形膠質(zhì)細胞是中樞神經(jīng)系統(tǒng)中最豐富的非神經(jīng)元細胞類型;如果沒有星形膠質(zhì)細胞的密切作用,神經(jīng)元就無法在大腦中生存。因此,星形膠質(zhì)細胞的功能可嚴(yán)重影響缺血后神經(jīng)元的存活。因此,防止星形膠質(zhì)細胞損傷和死亡顯示了在缺血再灌注損傷后保護大腦的相當(dāng)大的治療潛力。通過模擬缺血再灌注損傷,建立OGD/R誘導(dǎo)的體外星形膠質(zhì)細胞損傷模型。在本研究中,蘇合香通過提高細胞活力和降低LDH釋放,對OGD/R誘導(dǎo)的星形膠質(zhì)細胞損傷具有保護作用(圖1A,B)。在哺乳動物中,細胞內(nèi)[Ca2+]先于ROS水平激增,而ROS水平的激增似乎對腦缺血-再灌注損傷至關(guān)重要,此前的研究表明,ROS可增加缺血-再灌注過程中線粒體通透性過渡孔的開放。如圖1C所示,OGD/R誘導(dǎo)細胞內(nèi)ROS生成顯著增加,而蘇合香誘導(dǎo)細胞內(nèi)ROS生成顯著降低。這些數(shù)據(jù)表明,蘇合香能夠保護星形膠質(zhì)細胞免受OGD/R損傷。
炎癥在缺血性腦損傷病理中起著重要作用。腦缺血引起明顯的炎癥反應(yīng),其特征是黏附分子、趨化因子和細胞因子的釋放和激活,從而加重腦損傷。有證據(jù)表明,促炎細胞因子如IL-6、IL-1β和TNF-α是缺血性腦損傷急性期反應(yīng)性星形膠質(zhì)細胞的初始觸發(fā)因子。此外,反應(yīng)性星形膠質(zhì)細胞會分泌不同的促炎細胞因子和黏附分子,如ICAM-1、VCAM-1、IL-6、IL-1β、TNF-α等,可能參與了一個循環(huán)不斷激活的過程。因此,減少激活的星形膠質(zhì)細胞引起的炎癥反應(yīng)可以預(yù)防腦缺血后的神經(jīng)炎癥。我們的研究表明,OGD/R損傷可引發(fā)炎癥,星形膠質(zhì)細胞中黏附分子和促炎細胞因子如ICAM-1、VCAM-1、IL-6、IL-1β、TNF-α的表達增加,而蘇合香則抑制了這些黏附分子和促炎細胞因子的表達(圖2)。這些數(shù)據(jù)表明蘇合香可以減少OGD/R損傷的星形膠質(zhì)細胞中炎性細胞因子和黏附分子的釋放;此外,還掩蓋了黏附分子和促炎細胞因子誘導(dǎo)的星形膠質(zhì)細胞激活。
NF-κB是一種轉(zhuǎn)錄因子,在星形膠質(zhì)細胞的炎癥反應(yīng)中起重要作用,NF-κB的激活是編碼促炎細胞因子的基因轉(zhuǎn)錄所必需的。NF-κB家族由5個不同的成員組成,分別是p50、p52、p65、c-Rel和Rel-B。p65的磷酸化被廣泛研究為NF-κB激活形式,有助于穩(wěn)定核內(nèi)NF-κB復(fù)合物,促進神經(jīng)系統(tǒng)基因表達。NF-κB的活化開始于磷酸化,隨后κB抑制劑(IκB)的降解,進而導(dǎo)致游離NF-κB從細胞質(zhì)轉(zhuǎn)位到細胞核,促進促炎基因的表達。事實上,缺血性損傷后,星形膠質(zhì)細胞NF-κB信號通路的失活會減少細胞因子的產(chǎn)生并保護神經(jīng)元。在本研究中,我們觀察到OGD/R增強了星形膠質(zhì)細胞中IκBα的降解、NF-κB磷酸化以及活性NF-κBp65從細胞質(zhì)到細胞核的轉(zhuǎn)位,而蘇合香減弱了這些NF-κB的變化(圖3)。蘇合香介導(dǎo)的活性依賴于NF-κB的激活。使用NF-κB特異性抑制劑BAY11-7082可以部分阻止蘇合香對細胞活力和神經(jīng)毒性的影響(圖4),表明NF-κB活化在蘇合香介導(dǎo)的OGD/ r損傷星形膠質(zhì)細胞保護中發(fā)揮關(guān)鍵作用。
在這項工作中有幾個注意事項和限制。首先,蘇合香的成分非常復(fù)雜,主要成分包括游離肉桂酸、苯乙烯酸(肉桂酸酯)、苯丙基肉桂酸酯、由三萜酸(齊墩果酸和3-烯齊墩果酸)及其肉桂酸酯組成的樹脂(蘇合香樹脂)和揮發(fā)油。進一步的實驗來證實蘇合香的神經(jīng)保護成分在臨床上是很重要的。其次,星形膠質(zhì)細胞功能在缺血時對神經(jīng)元存活有重要影響,蘇合香是否能通過星形膠質(zhì)細胞保護神經(jīng)元,神經(jīng)元與星形膠質(zhì)細胞之間的相互作用,其分子病理機制有待進一步明確。
綜上所示,蘇合香通過激活NF-κB信號通路,減輕炎癥細胞因子的表達,保護OGD/R損傷的初級皮層星形膠質(zhì)細胞。進一步研究蘇合香中神經(jīng)保護的關(guān)鍵成分及其與NF-κB的作用機制具有重要意義。
參考文獻:
[1] Xu Zhuo, Lu Danni, Yuan Jianmei, Ren Mihong, Ma Rong, Xie Qian, Li Yong, Li Jinxiu, Wang Jian. Storax, A Promising Botanical Medicine for Treating Cardio-Cerebrovascular Diseases: A Review. Frontiers in Pharmacology, 2021, 12, DOI.10.3389/fphar.2021.785598
[2] Zhang Meng, Ma Yan, Chai Lijuan, Mao Haoping, Zhang Junhua, Fan Xiang.Storax Protected Oxygen-Glucose Deprivation/Reoxygenation Induced Primary Astrocyte Injury by Inhibiting NF-κB Activation in vitro.Frontiers in Pharmacology, 2019, 9, DOI.10.3389/fphar.2018.01527