服務熱線
177-5061-9273

覆盆子酮,又稱樹莓酮,是一種天然酚類化合物,是紅樹莓的主要芳香化合物。
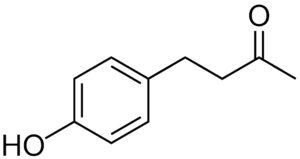
覆盆子酮的結構式
Preferred IUPAC name:4-(4-Hydroxyphenyl)butan-2-one
Other names: p-Hydroxybenzyl acetone; 4-(p-Hydroxyphenyl)-2-butanone; Frambinone; Oxyphenylon; Rheosmin; Rasketone
來源
覆盆子酮存在于多種水果中,包括樹莓、蔓越莓和黑莓。它是由香豆酰輔酶a生物合成的。它可以從果實中提取,每公斤樹莓的產量約為1-4毫克。

樹莓(Raspberry)
制備
由于覆盆子酮的天然豐度很低,工業上通過多種方法從化學中間體中制備覆盆子酮。其中一種方法是通過交叉醛醇縮合,然后催化氫化。首先,丙酮與4-羥基苯甲醛縮合形成α、β不飽和酮。然后烯烴部分被還原成烷烴。這種兩步法生產覆盆子酮的產量為99%。硼化鎳是一種較便宜的加氫催化劑,它對烯酮雙鍵的加氫也表現出較高的選擇性。
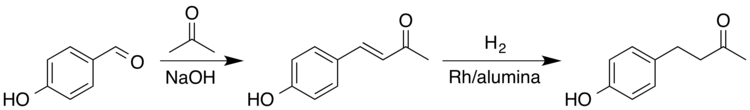
應用
覆盆子酮有時用于香水、化妝品和食品添加劑,以增加水果味。它是食品工業中使用的最昂貴的天然香料成分之一。這種天然化合物的價格高達每公斤2萬美元。合成覆盆子酮更便宜,估計每磅幾美元到天然產品成本的五分之一不等。雖然含有這種化合物的產品被用于減肥,但沒有臨床證據表明這種效果在人類身上可以顯現。
安全性
人們對覆盆子酮補充劑的長期安全性知之甚少,尤其是在人類身上做的研究很少。因為它在化學上與興奮劑辛弗林有關,所以它的安全性存在一些問題。毒理學模型表明潛在的心臟毒性作用,以及對生殖和發育的影響。此外,在許多含有覆盆子酮的膳食補充劑中,制造商添加了其他成分,如咖啡因,可能有不安全的影響。1965年,美國食品和藥物管理局將用于調味食品的少量覆盆子酮歸類為公認的安全(GRAS)。
覆盆子酮的生物合成
1、工程大腸桿菌共表達生姜酮合成酶和葡萄糖脫氫酶高效合成覆盆子酮 [1]
覆盆子酮(RK)是樹莓果實的主要芳香化合物,在化妝品、食品和醫藥等領域有著廣泛的應用。在本研究中,我們通過使用全細胞生物催化劑催化還原對羥基芐叉丙酮來生物合成RK。在大腸桿菌中表達芽孢霉的還原酶RiRZS1和嗜酸熱漿菌的葡萄糖脫氫酶SyGDH,再生NADPH進行全細胞催化反應。通過平衡兩種酶在pRSFDuet-1中的共表達,我們獲得了9.89 g/L的RK,轉化率為98%,時空產率為4.94 g/(L·h)。最適條件為40℃,pH 5.5,底物與輔助底物的摩爾比為1:2.5。本研究結果為RK的生物合成提供了一種有前景的方法。
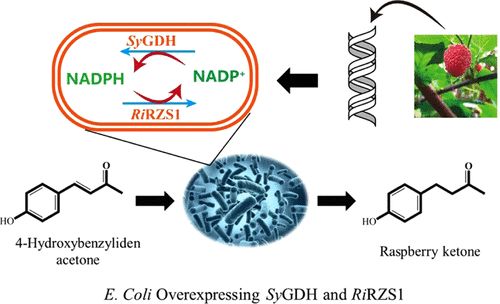
圖1 工程大腸桿菌共表達生姜酮合成酶和葡萄糖脫氫酶高效合成覆盆子酮
2、通過幾種不相關的植物細胞培養實現覆盆子酮的生物轉化 [2]
生物轉化,即利用生物系統在溫和條件下對合成或天然化合物進行化學合成,是生產新的活性或高價值化合物的一種有吸引力的工具。植物細胞顯示出巨大的生化潛力,能夠通過酶的過程轉化一系列物質,包括藥物成分和工業副產品。植物細胞培養的使用為控制和優化生產過程提供了可能性,可應用于工業規模。覆盆子酮[4-(4-羥基苯基)丁烷-2-酮]是最有趣的天然香料化合物之一,因其高需求和巨大的市場價值。這種與工業相關的風味化合物的生物合成具有較好的表征,它包括3型聚酮合酶將4-香豆酰輔酶a和丙二酰輔酶a縮合成二酮,然后由NADPH依賴性還原酶催化還原。覆盆子酮已成功地利用不同的宿主和前體進行生物轉化,建立了更有效和經濟的過程。本實驗研究了煙草中過表達RiZS1對覆盆子酮前體生物轉化的影響。此外,研究了各種野生型植物細胞培養物以4-羥基亞芐基丙酮或樺木醇為底物進行覆盆子酮生物轉化的能力。顯然,植物細胞具有相當廣泛分布的還原酶活性,能夠利用廉價和易得的前體進行生物轉化為覆盆子酮。
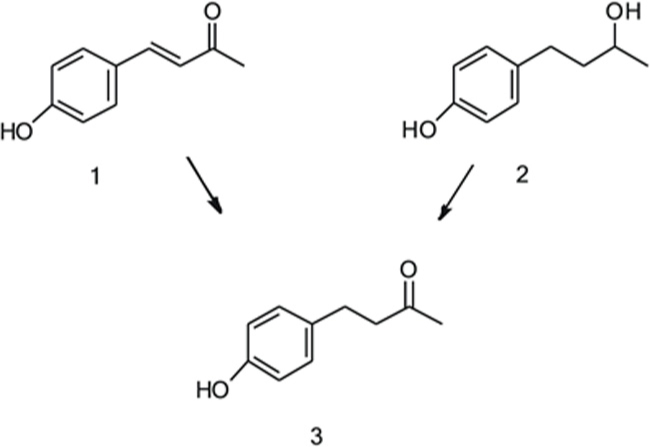
圖2 4-羥基亞芐基丙酮(1)和樺木醇(2)轉化樹莓酮(3)
樹莓衍生的前體化合物1在自然界并不豐富,但可以通過羥基苯甲醛和丙酮的縮合細菌培養產生。化合物2是一種從紅豆杉(Taxus wallichiana)中分離得到的二級醇。在樺樹皮、杜鵑、赤楊、楓樹和冷杉中也發現了這種物質,主要以糖基化形式存在,稱為白樺糖苷。白樺糖苷可以通過微生物β-葡萄糖苷酶轉化為白樺黃素。化合物2轉化為3已經被各種微生物細胞和顛茄毛根成功地實現。在Kosjek et al.(2003)的一項研究中,放線菌紅球菌(actinomycete Rhodococcus)利用丙酮作為氫受體進行了從2到3的氧化反應。然而,當顛茄毛狀根被加入底物2時,化合物3和白樺糖苷都可以在不需要額外的輔助基質的情況下形成。另一方面,Fujita et al.(1998)表明毛果槭(Acer nikoence)愈傷組織培養可以轉化化合物3到2和它們的糖苷。有趣的是,3只存在于培養基中,而糖苷則存在于細胞內空間。作者認為,某種特定的醇脫氫酶(ADH)和糖基轉移酶參與了這些反應。化合物1的生物轉化通過各種微生物細胞完成,產生具有不同轉化效率的覆盆子酮。他們觀察到,隨著孵化時間的延長,1到3的轉化可以伴隨2的生成。已知從1到3的反應是由一種依賴NADPH的酶催化的,這種酶是Koeduka等人(2011)從覆盆子(Rubus idaeus)中鑒定出來的。另一方面,從2到3的轉化過程還沒有被確定。事實上,Beekwilder等人(2007)表明,大腸桿菌在向表達亞芐基丙酮合成酶(BAS)的細胞注入p-香豆酸后,具有內源性還原酶活性,可將1轉化為3。因此,這種轉化所需的還原酶活性很可能在自然界中分布得相當廣泛。在本研究中,我們介紹了與覆盆子酮相關的生物轉化研究,研究對象是來自與覆盆子無關的植物的各種植物細胞培養。
3、高價值精細化學品覆盆子酮的高產“一鍋法”生物合成 [3]
無細胞萃取物和基于純化酶的系統為研究一系列化學物質的生物合成策略提供了一個有吸引力的解決方案。4-(4-羥基苯基)丁烷-2-酮,又稱覆盆子酮,是樹莓果實的主要香味成分,是食品和運動行業的天然添加劑。目前,自然形態的覆盆子酮的工業加工涉及到從產量為~ 1 - 4毫克每公斤的果實中進行化學提取。由于毒性,微生物生產只能提供高達5-100 mg /L的低產量。在此,我們報道了一種高效的無細胞策略,以探索一種合成酶途徑,將L-酪氨酸或其前體4-(4-羥基苯基)-丁烯-2-酮轉化為覆盆子酮,轉化率高達100%。作為這一策略的一部分,廉價回收輔助因子是必要的。具體來說,該途徑的最后一步酶是由覆盆子酮/姜酮合酶(RZS1)催化的,這是一種依賴于NADPH的雙鍵還原酶。為了放松輔助因子對NADH(游離細胞生物合成的首選輔助因子)的特異性,我們鑒定了一種與NADH具有強烈活性的異構酶(G191D)。我們在“一鍋”無細胞反應中實現了RZS1 G191D異構,以高產量(61 mg/L)生產覆盆子酮,這為傳統微生物生產提供了一種替代途徑。總之,我們的無細胞策略補充了對工程合成酶級聯到工業相關的增值化學品的日益增長的興趣。
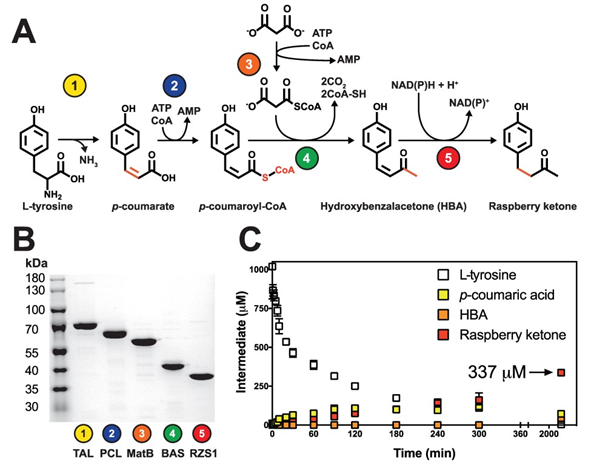
圖3 覆盆子酮無細胞生物合成的模塊。從L-酪氨酸到丙二酸合成覆盆子酮的合成途徑。B.合成路徑上酶的SDS-PAGE。2 μg酶純化后,進行12% (v/v) SDS-PAGE和考馬斯亮藍染色分析。his6標記重組酶- r的大小。粘蟲(glutinis TAL) (77.0 kDa)、擬南芥(A. thaliana PCL) (63.2 kDa)、沼澤沙鼠(R. palustris MatB) (56.6 kDa)、掌葉沙鼠(R. palmatum BAS) (44.4 kDa)、紅沙鼠RZS1 (40.7 kDa)。C.用2.5 μM酶在標準條件下一鍋法合成覆盆子酮。LC-MS測定的中間體包括L-酪氨酸(白框)、p-香豆酸酯(黃框)、HBA(橙框)和覆盆子酮(紅框)。數據代表三次實驗重復。
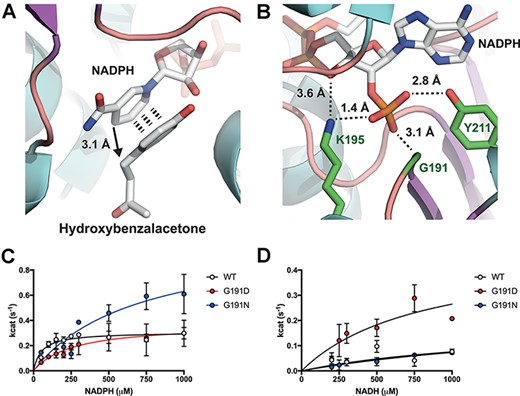
圖4 基于結構工程的RZS1還原酶的NADH特異性增加(pdb: 6EOW)。A.接近NADPH輔助因子的HBA的結合位點。B.輔助因子特異性是由G191, K195和Y211三個結合殘基提供的,它們與5個?-磷酸核糖氫鍵結合。C. RZS1 G191異構的NADPH動力學。D. RZS1 G191異構的NADH動力學。
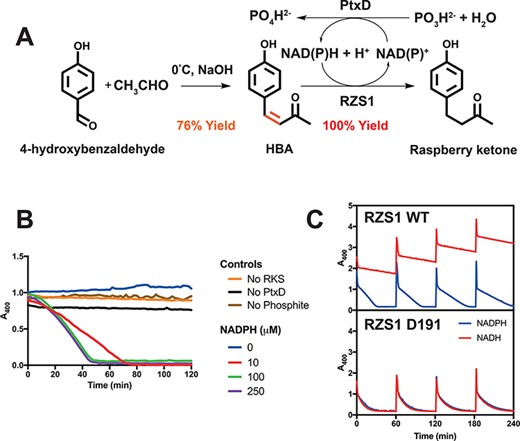
圖5 利用NADH和輔助因子再生兩步法合成覆盆子酮。A.一種利用醛醇縮合和RZS1還原酶活性及輔助因子再生的覆盆子酮半合成途徑。B.高溫PtxD opt12亞磷酸脫氫酶的活性:1 mM HBA和10 μM RZS1。陰性對照(無酶或亞磷酸)與不同濃度的NADPH一起顯示。C. 400 nm時程反應監測吸光度損失,顯示對羥基苯甲醛(HBA)還原為覆盆子酮。每60分鐘注射1 mM HBA。過量的PtxD和20 mM亞磷酸鹽與10 μM RZS1(上面板)或D191異構酶(下面板)在30°C孵育,與0.25 μM NADPH(藍線)或NADH(紅線)。
無細胞合成生物學和合成生物化學的相關領域提供了一個令人興奮的機會來設計和設計活細胞之外的酶途徑。最近的進展包括合成CO2固定循環的產生和20 000 L的肌醇生物合成。天然產品和其他高價值的精細化學品通常只在其天然來源中以非常低的濃度合成。因此,人們對開發一系列高價值精細化學品的生物可持續合成路線的興趣日益增加。至于覆盆子酮,樹莓本身只合成了少量,而且這個過程需要數周的成熟期。雖然覆盆子酮中間體一般會抑制微生物生長,但使用大腸桿菌全細胞(固定相細胞)生物催化劑系統可以繞過這一過程,該系統的活性達到g/L級,但需要化學衍生的前體對羥基苯甲醛(HBA)。另外,可以從天然原料中提取的底物L-酪氨酸或對香豆酸鹽,可以在本文所述的III型聚酮中,在合成工程大腸桿菌和釀酒酵母系統中轉化,但由于一般毒性,產量有限(高達95 mg/L)。
在此,我們研究了一種可替代的無細胞“一鍋”多酶系統的生物合成覆盆子酮。覆盆子酮是一種較為簡單的聚酮類化合物,其生物合成途徑仍然需要昂貴的輔助因子ATP、丙二酰輔酶a和NAD(P)H。通過研究細胞外的這個系統,可以精確控制酶水平,并靈活測試不同的輔助因子循環系統。我們證明了覆盆子酮可以從L-酪氨酸的五步法合成,但是,最經濟的輔助因子NADH的產量有限。因此,為了降低關鍵的成本因子NADPH,我們的工作重點是放松RZS1雙鍵還原酶對NADH的輔助因子特異性。許多研究強調,NADPH氧化還原酶可以被設計成使用更穩定和廉價的NADH或仿生類似物。作為一種廣義的方法,NAD(P)H酶的結構導向設計可以通過改變對核糖5?-磷酸(NADPH)或羥基(NADH)基團的親和力來實現。在RZS1酶的情況下,G191的空間結構為結合特異性寬松的輔助因子提供了靈活的控制。它通過亞磷酸脫氫酶與廉價的磷酸鹽供體結合使用,從而提供了在無細胞條件下利用NADH使用所述的三種起始底物中的任何一種低成本合成覆盆子酮的途徑。重要的是,RZS1 G191D異構酶在低水平的NADH (10 μM)下是有效的,并能保持數天的活性。通過將該酶代入完整的“一鍋”多酶體系,我們可以在一個批處理體系中獲得61 mg/L的覆盆子酮,底物L-酪氨酸(300 μM或54 mg/L)完全轉化為覆盆子酮。在較高濃度的L-酪氨酸,盡管試圖優化輔助因子和ATP水平(數據未顯示),我們觀察到合成途徑上的中間體和副產物bisnoryangonin的積累。最后,我們也證明了一種有效的兩步化學酶法合成覆盆子酮。這類似于Yang等人所采用的策略,即由于化學合成對羥基苯甲醛HBA的要求,獲得了“天然等同”且經濟價值較低的產品。因此,如果可擴展性得到證明,制備天然覆盆子酮的五步法將更有意義。然而,需要進一步的亞芐基丙酮合成酶(benzalacetone synthase, BAS)酶工程,表征新的亞芐基丙酮合成酶同源物,或開發替代的酶途徑。這是因為在我們優化的反應中,亞芐基丙酮合成酶的催化活性是限速的,而且它還會產生一種不希望的副產物bisnoryangonin。
雖然全面的技術經濟分析超出了目前工作的范圍,但用無細胞酶的方法進行精細化學合成可以在可持續性方面提供好處。目前,用于化妝品和食品添加劑的精細化工市場中,大約80%是由石油衍生的化學合成生產的,因此,如果聲明為“天然等同”,就可以被批準使用。因此,對于從需要大量農業用地的食物來源中自然提取的精細化學物質,通過使用轉基因植物和微生物或通過擴大無細胞系統,設計更綠色的替代生物催化平臺可能更簡單、更可持續。與全細胞生產工藝相比,使用純化酶可能在控制副反應方面提供好處,由于較少的代謝物污染而易于純化,或在產品毒性限制細胞生長的情況下。然而,酶生產和純化的成本,以及添加昂貴的輔因子(通常由細胞內的培養基成分產生)的需要,確實導致了成本的增加。諸如酶的固定化以實現回收和再利用的策略,可能被用來實現經濟可行性。
在這里,我們使用覆盆子酮作為一個模型途徑,展示了一個明顯的非生產性酶途徑可以從細胞外設計到一個高水平產量的性能。這一過程的關鍵是在完成過程中研究途徑酶的能力,而不是作為單個不耦合動力學,因為共享資源(CoA, ATP)可以影響總產量。總之,無細胞合成生物學提供了一個可擴展的機會來設計合成酶的合成器與輔助因子的有效性一致。我們已經應用這種合理的方法來優化覆盆子酮,這是一種小分子,不易從工程活細胞中獲得。在未來,具有高度穩定和活性酶的大規模無細胞工程方法,有潛力在與傳統的細胞工程競爭中發揮更廣泛的作用,特別是在高價值的精細化學品、重組蛋白和天然產品方面。
覆盆子酮的藥理活性
1、覆盆子酮作為天然抗氧化劑的潛力 [4]
氧化應激與各種疾病密切相關,許多研究已經確定如何減少這種應激。特別是,人們正在努力從天然產品中尋找潛在的抗氧化劑。研究表明覆盆子酮(RK;4-(4-羥基苯基)-2-丁酮具有多種藥理活性。本文就RK的抗氧化活性及其作用機制進行綜述。在幾個實驗模型中,證明了RK通過增加總抗氧化能力(TAC)來顯示抗氧化性能;上調抗氧化酶,如超氧化物歧化酶(SOD)和過氧化氫酶(CAT);改善脂質過氧化。綜上所述,RK抗氧化活性的研究與其他各種生理活性有直接或間接的關系。進一步的臨床研究將證實RK作為一種有效的抗氧化劑、功能性保健食品和治療劑的價值。
還需要對RK的安全性和毒性進行更廣泛的評價。根據調味料制造商協會(FEMA)的標準,RK被授予GRAS(公認為安全)地位,并被美國食品和藥物管理局(FDA)批準用于食品用途(21 CFR 172.515),對公眾健康沒有危害。RK對雄性和雌性大鼠急性口服半數致死量(LD50)分別為1.32 g/kg和1.40 g/kg。此外,除了短暫的血紅蛋白下降外,喂食0.1-1.0% RK的飼料13周后,所有大鼠均未出現明顯的亞急性毒性,包括體重增加。根據這些數據,RK目前作為一種減肥膳食補充劑在市場上銷售,推薦劑量為100 - 1400毫克/天。然而,一些研究人員仍然警告過度使用RK補充劑的風險,因為RK的安全性和毒性尚未得到充分評估,特別是在高劑量情況下。在最近的一項研究中,急性單次口服640mg/kg RK可引起C57BL/6J小鼠的各種病理改變,包括白色脂肪組織萎縮、脾異常、胸腺退化和某些血液學值升高。進一步研究RK的慢性毒性及其對人體的有害影響,將有助于建立更安全的臨床使用RK的給藥方案。

圖6 覆盆子酮的生物活性示意圖
2、覆盆子酮的潛在代謝活性 [5]
近年來,新型食品和食品復合干預手段在預防和治療代謝性疾病方面引起了人們的廣泛關注。覆盆子酮(RK)是一種芳香化合物,存在于紅色水果和漿果中,已被用作非處方藥的減肥產品。然而,實際上,RK對減肥的影響仍存在爭議,其機制在很大程度上還不清楚。此外,體內和體外研究表明,RK對其他代謝性疾病的發展具有有益作用。本文綜述了RK的合成、生物利用度、代謝等方面的研究進展,并對其抗肥胖、抗糖尿病、保護心臟、保護肝臟等潛在生物活性及其作用機制進行了綜述。本文概述了目前的研究結果,并提出了RK在人類健康領域的未來研究。覆盆子酮(RK)被用于控制體重已有多年,但考慮到食物攝入量,這種效果存在爭議。此外,RK對T2DM、肝和心臟損傷也有好處。RK的保護作用機制包括促進脂肪酸氧化、平衡血糖水平、抗炎、抗氧化等。在這方面,我們對RK對許多代謝性疾病的益處進行了全面的分析,并討論了其潛在的分子機制。希望我們的工作對進一步研究RK,提高公眾對RK的認識有所幫助。
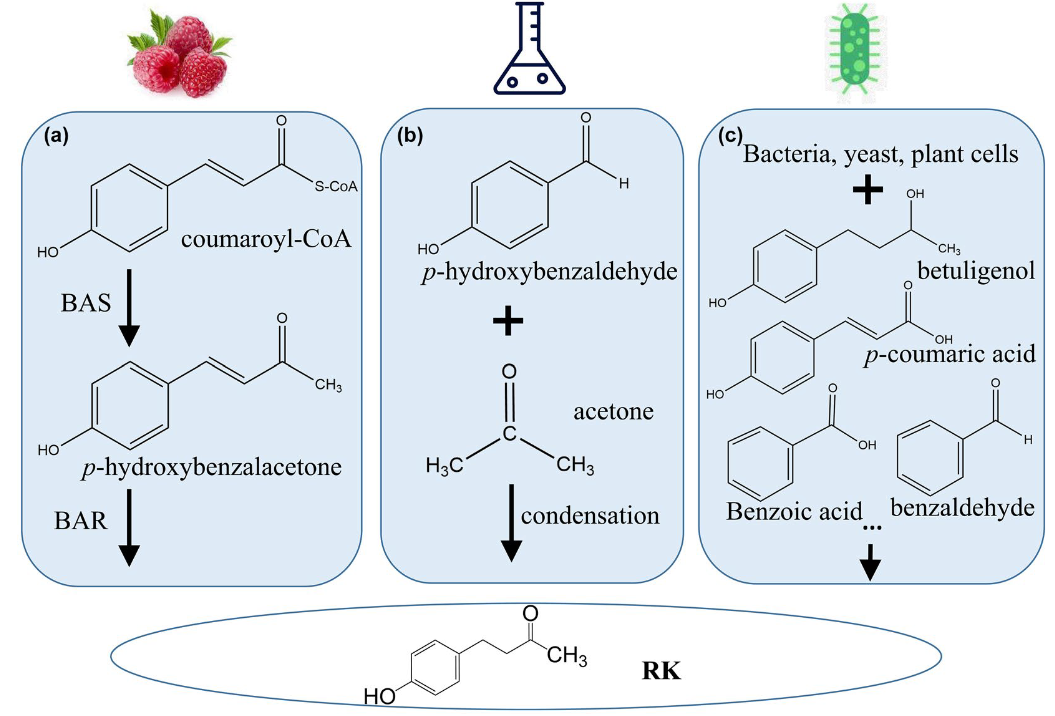
圖7 植物,化學和微生物合成覆盆子酮的反應路徑
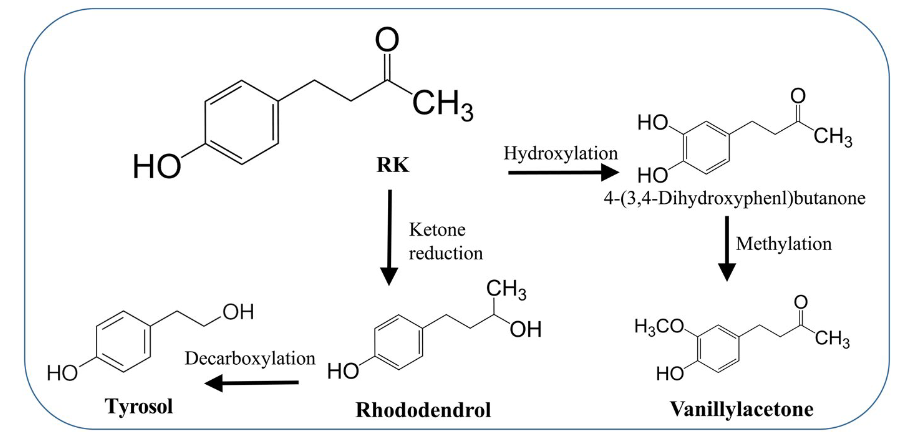
圖8 老鼠胞漿中覆盆子酮的轉化及其主要代謝產物
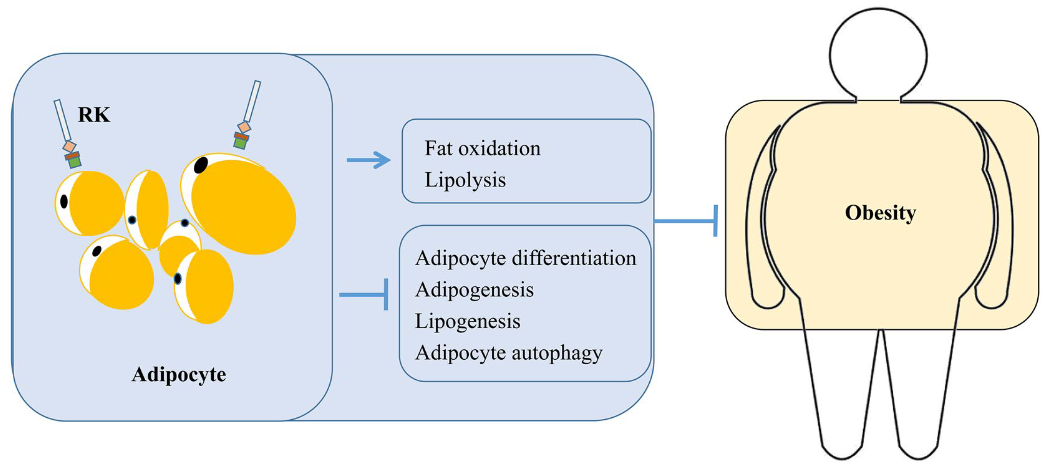
圖9 覆盆子酮通過調控脂肪細胞來控制人的體重
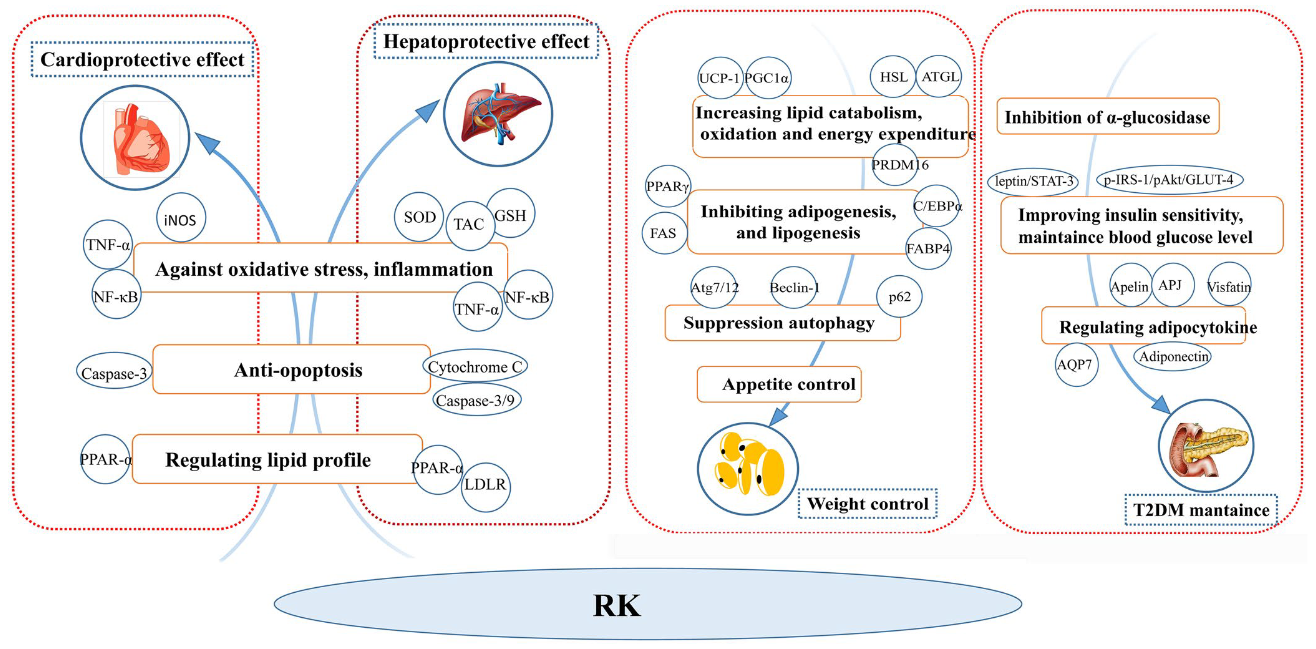
圖10 覆盆子酮在代謝性疾病中的作用
3、酚類化合物藥理研究:覆盆子酮2020年更新 [6]
覆盆子酮(RK)是一種芳香酚類化合物,天然存在于紅樹莓、獼猴桃、桃子和蘋果中,并被報道具有潛在的治療和營養特性。細胞和嚙齒類動物的研究表明,RK在肝臟/心臟/胃的保護中發揮重要作用,并作為一種抗高脂血癥、抗肥胖、脫色和性成熟劑。覆盆子酮介導的過氧化物酶體增殖物激活受體-α (PPAR-α)的激活是其主要的作用方式之一。雖然嚙齒類動物研究已經證實了RK的有效作用,但其作用機制仍在很大程度上未知。盡管缺乏可靠的人體研究,RK作為一種健康補充劑在市場上銷售,劑量非常高。在這篇綜述中,我們提供了迄今為止進行的科學研究的匯編,評估RK在幾種疾病條件下的治療特性,并在RK被認為是治療主要生活方式疾病的一種安全有效且副作用有限的替代藥物之前,啟發未來的研究。
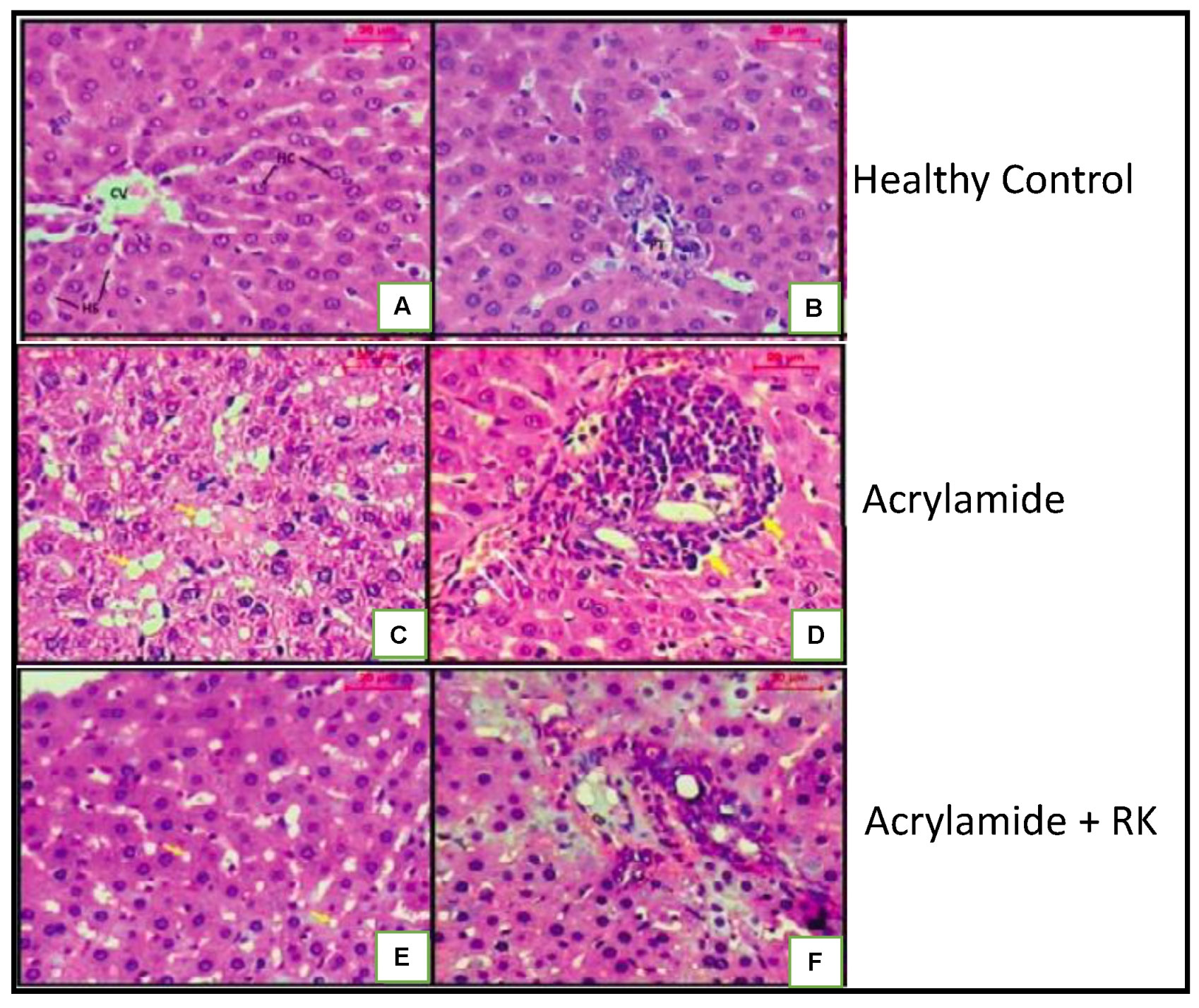
圖11 RK介導的丙烯酰胺性肝病大鼠肝臟保護作用健康對照組肝臟切片的顯微照片(A,B),顯示正常的肝小葉結構。中央靜脈被肝細胞、肝竇和正常的門靜脈所包圍。(C,D)丙烯酰胺處理組肝切片顯示肝小葉紊亂,肝細胞內空泡,門靜脈內大量淋巴細胞浸潤,門靜脈周圍腔擴張充血。(E,F) RK-丙烯酰胺處理組的肝小葉看起來或多或少像正常;門管區伴輕度浸潤,肝細胞基本正常。他走時染色;比例尺:20mm。
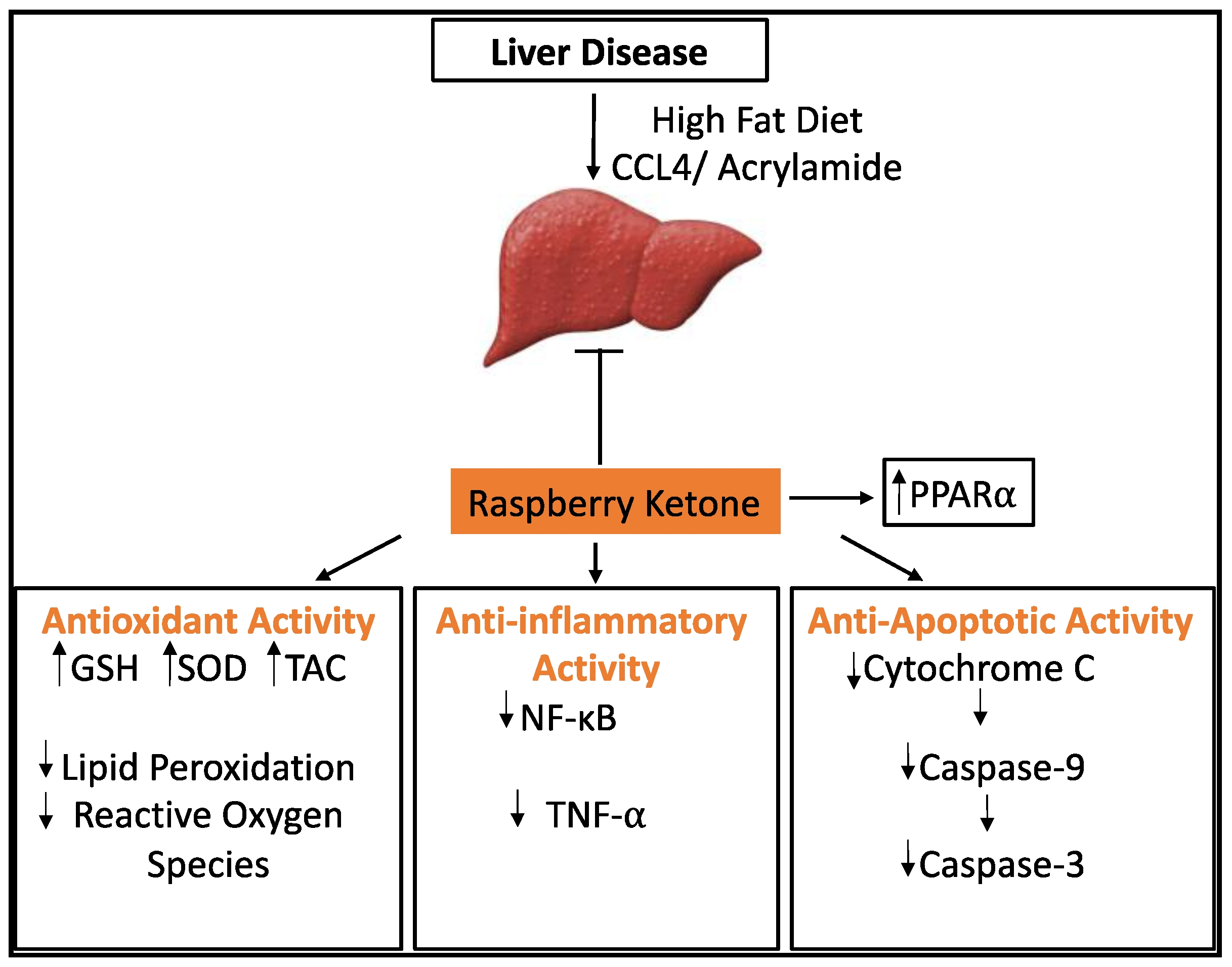
圖12 RK對由高脂肪飲食、CCL4或丙烯酰胺引起的肝臟疾病的保護作用。
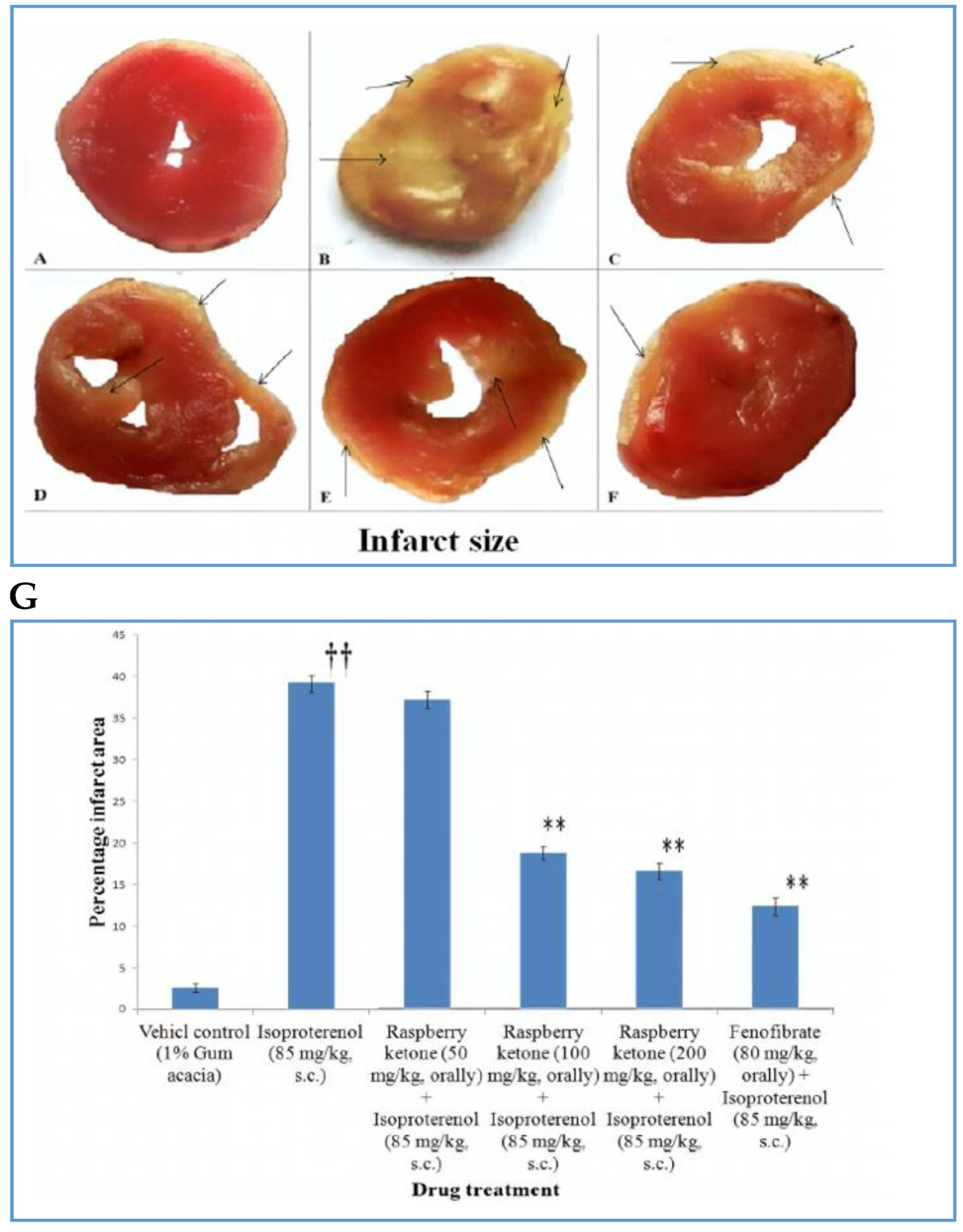
圖13 RK及不同藥物對各組心肌梗死面積的影響(箭頭所示)。(一)空白對照阿拉伯樹膠(1%),(B)異丙腎上腺素(85毫克/公斤,南卡羅來納州)(C) RK(50毫克/公斤,口服)+異丙腎上腺素(85毫克/公斤,南卡羅來納州)(D) RK(100毫克/公斤,口服)+異丙腎上腺素(85毫克/公斤,南卡羅來納州)(E) RK(200毫克/公斤,口服)+異丙腎上腺素(85毫克/公斤,南卡羅來納州)(F)和非諾貝特(80毫克/公斤,口頭)+異丙腎上腺素(85毫克/公斤,南卡羅來納州)。圖中為不同處理組的梗死面積百分比(G),各柱為平均掃描電鏡(SEM)。通過單因素方差分析(one-way ANOVA)和Dunnett t檢驗確定顯著性:** p < 0.01與毒性對照;??p < 0.01與空白對照。
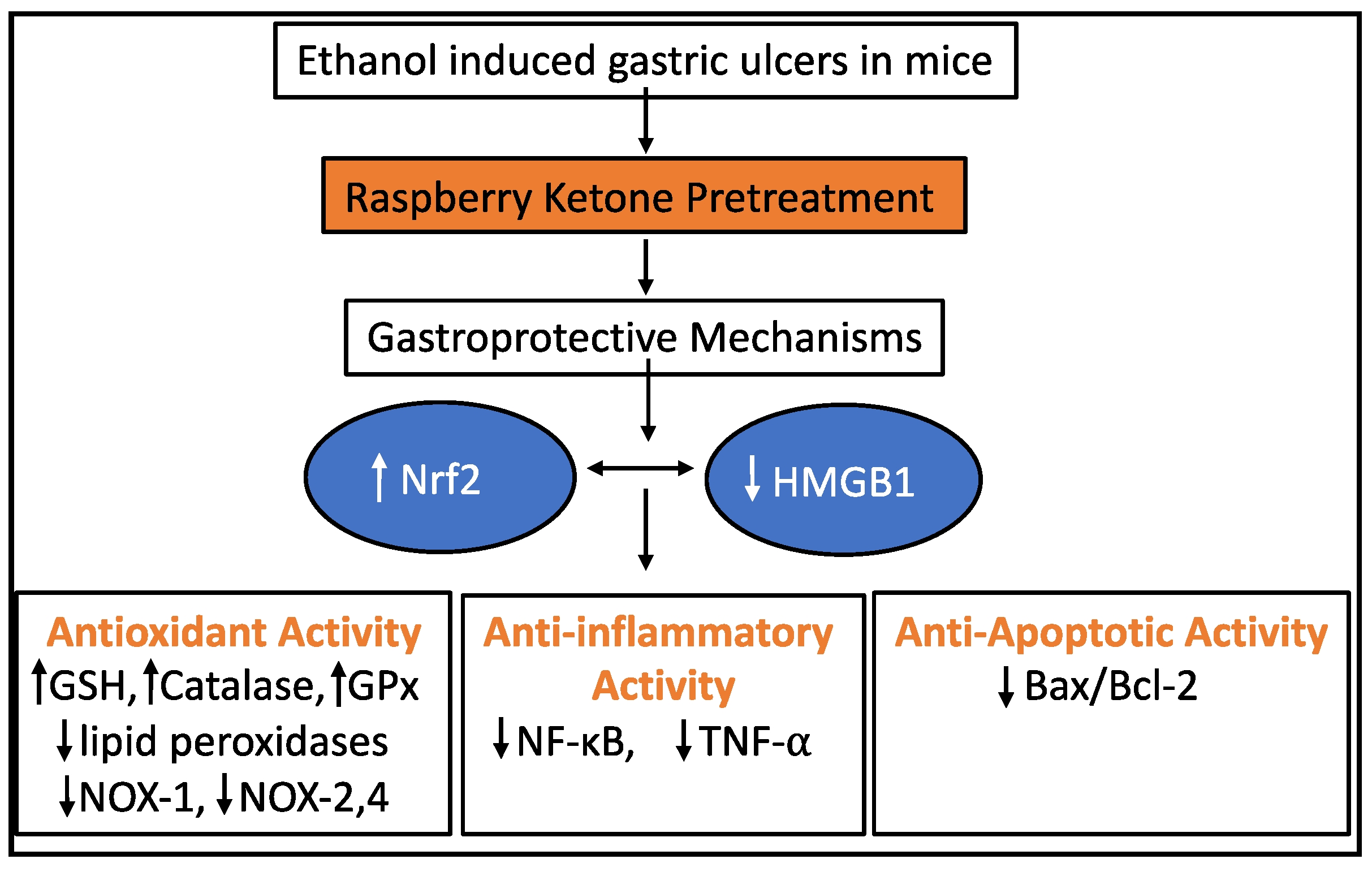
圖14 RK對乙醇誘導的大鼠胃潰瘍的胃保護作用的不同分子靶點示意圖。
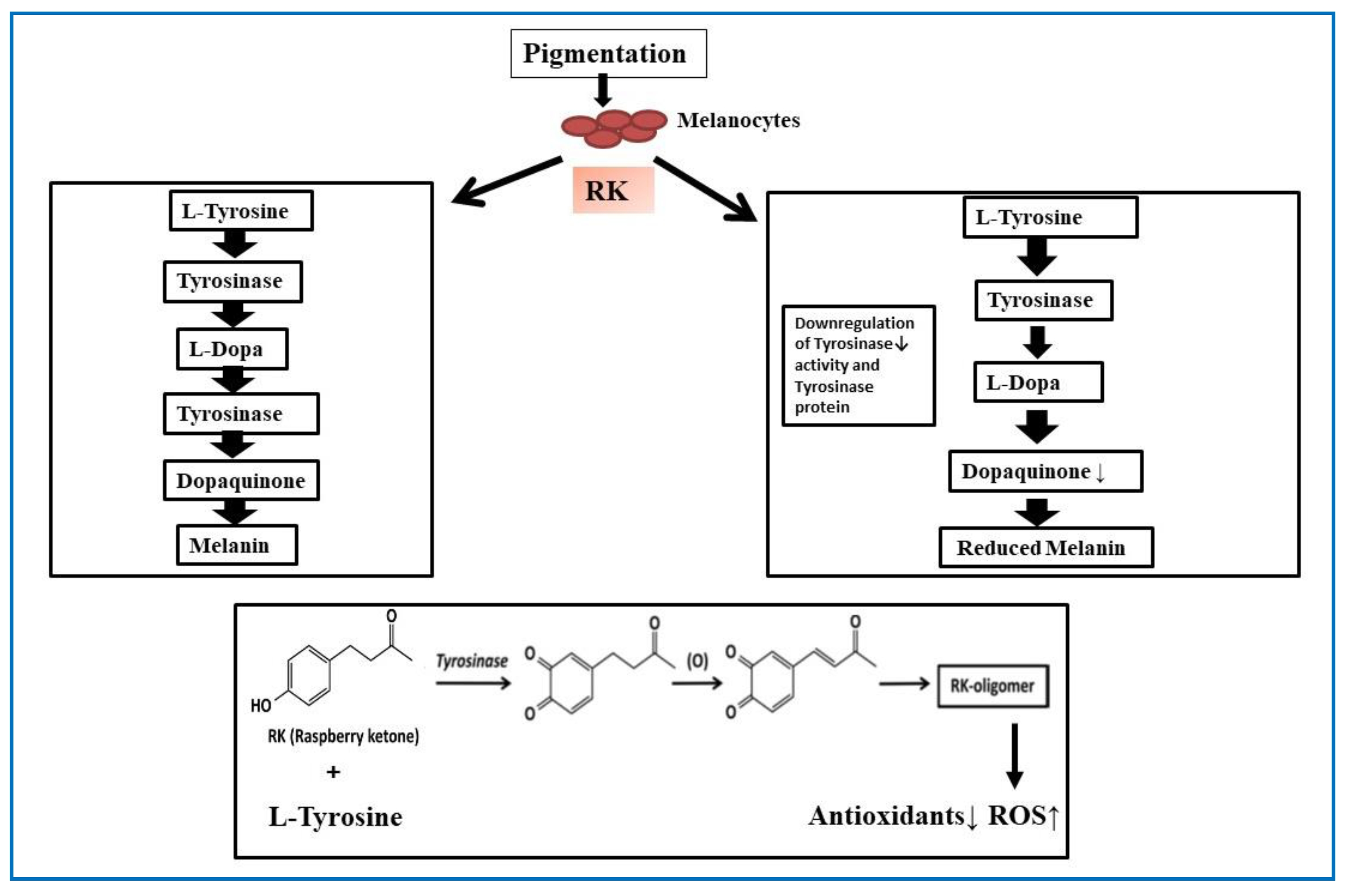
圖15 示意圖顯示黑色素細胞產生黑色素和RK對黑色素合成的影響,導致色素脫失(美白)。
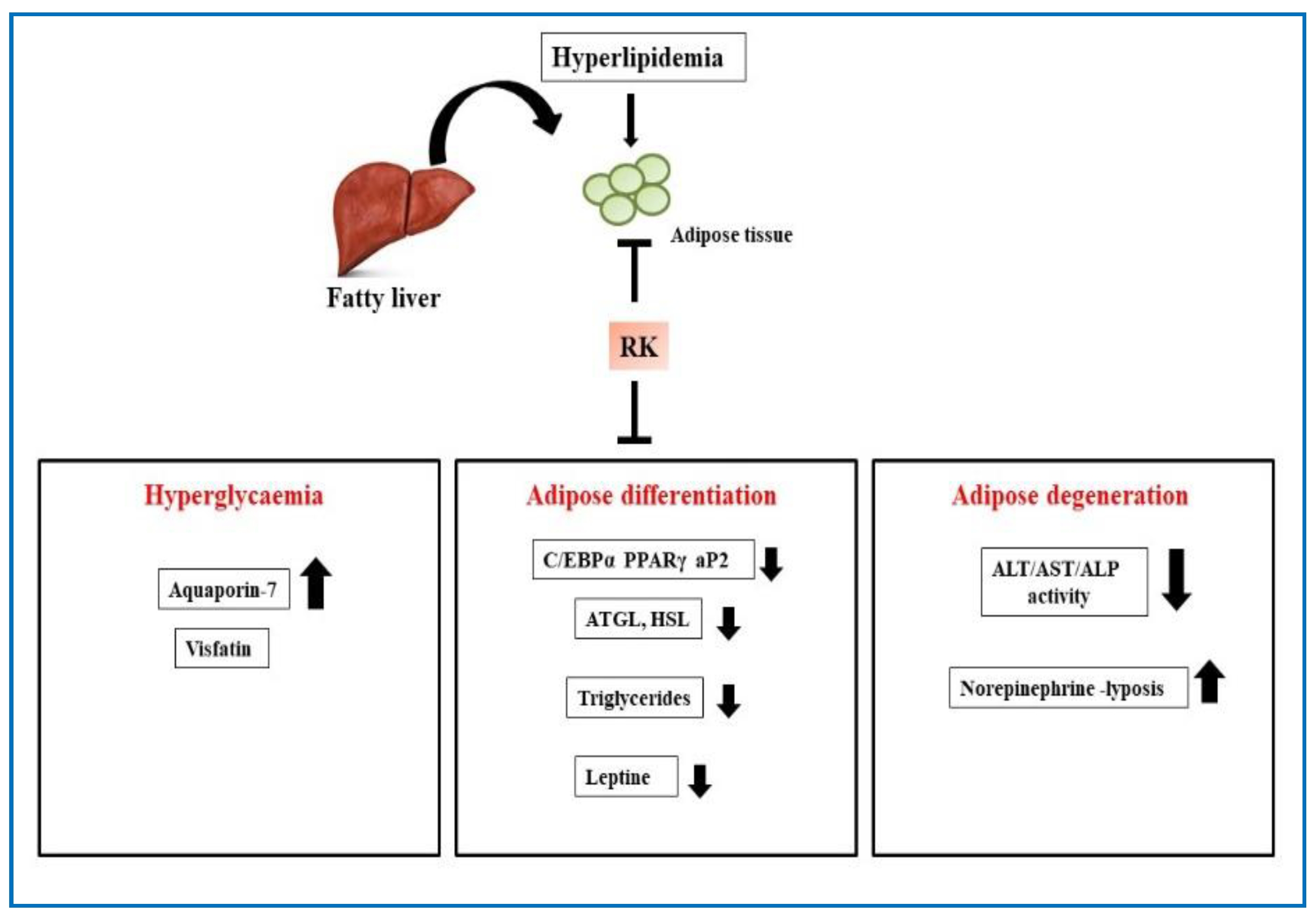
圖16 RK治療高脂血癥療效示意圖。

圖17 圖示昆蟲交配過程及RK在性成熟中的作用。
全世界對營養藥品的研究、生物活性成分的藥理探索及其治療各種疾病的潛力越來越感興趣。初步的體外和體內動物研究表明,RK在保護肝臟、保護心臟、治療胃潰瘍和肥胖等方面具有有益作用。然而,要將RK作為一種治療性分子,還需要進行大量的研究來確定其療效和作用機制。誠然,在未來的角度來看,RK可以被認為是導致一部分,識別并視為植物成分風格多樣化,有大量的治療和營養價值,但需要更嚴格的安全性和毒理學研究。覆盆子酮可以被認為是疾病治療前的預防性健康原料。我們希望目前對RK的全面綜述將作為基礎數據,以鼓勵對這一關鍵生物分子的進一步詳細研究,并使研究人員進一步探索和解開RK的其他特性,以幫助未滿足的臨床需求。
參考文獻
[1] Bo Yang, Pu Zheng, Dan Wu, and Pengcheng Chen. Efficient Biosynthesis of Raspberry Ketone by Engineered Escherichia coli Coexpressing Zingerone Synthase and Glucose Dehydrogenase. J. Agric. Food Chem. 2021, 69, 8, 2549–2556. https://doi.org/10.1021/acs.jafc.0c07697
[2] H?kkinen Suvi T., Sepp?nen-Laakso Tuulikki, Oksman-Caldentey Kirsi-Marja, Rischer Heiko. Bioconversion to Raspberry Ketone is Achieved by Several Non-related Plant Cell Cultures. Frontiers in Plant Science, 2015, 6, https://doi.org/10.3389/fpls.2015.01035.
[3] Simon J Moore, Tommaso Tosi, David Bell, Yonek B Hleba, Karen M Polizzi, Paul S Freemont, High-yield ‘one-pot’ biosynthesis of raspberry ketone, a high-value fine chemical, Synthetic Biology, Volume 6, Issue 1, 2021, ysab021, https://doi.org/10.1093/synbio/ysab021
[4] Lim SH, Choi C-I. Potentials of Raspberry Ketone as a Natural Antioxidant. Antioxidants. 2021; 10(3):482. https://doi.org/10.3390/antiox10030482
[5] Xiaoping Li,Teng Wei,Min Wu,Fang Chen,Peng Zhang,Ze-yuan Deng,Ting Luo. Potential metabolic activities of raspberry ketone. Journal of Food Biochemistry, 2022, 46(1),e14018. https://doi.org/ 10.1111/ jfbc. 4018
[6] Rao, Shailaja & Kurakula, Mallesh & Mamidipalli, Nagarjuna & Tiyyagura, Papireddy & Patel, Bhaumik & Manne, Ravi. (2021). Pharmacological Exploration of Phenolic Compound: Raspberry Ketone—Update 2020. Plants. 10. 1323. 10.3390/plants10071323.