服務熱線
177-5061-9273

諾卡酮,又稱圓柚酮,英文名Nootkatone,是一種天然有機化合物,是一種倍半萜類化合物,也是一種酮,是葡萄柚中最重要最昂貴的芳香物質,它也存在于其他生物體中。

諾卡酮賦予葡萄柚特有的柑橘味
以前,諾卡酮被認為是葡萄柚氣味和味道的主要化學成分之一。在高純度的情況下,它通常是無色的晶體。原油是液體,粘稠,呈黃色。諾卡酮通常是通過化合或生化氧化從葡萄柚中提取的。在阿拉斯加黃杉樹和香根草中都有發現。

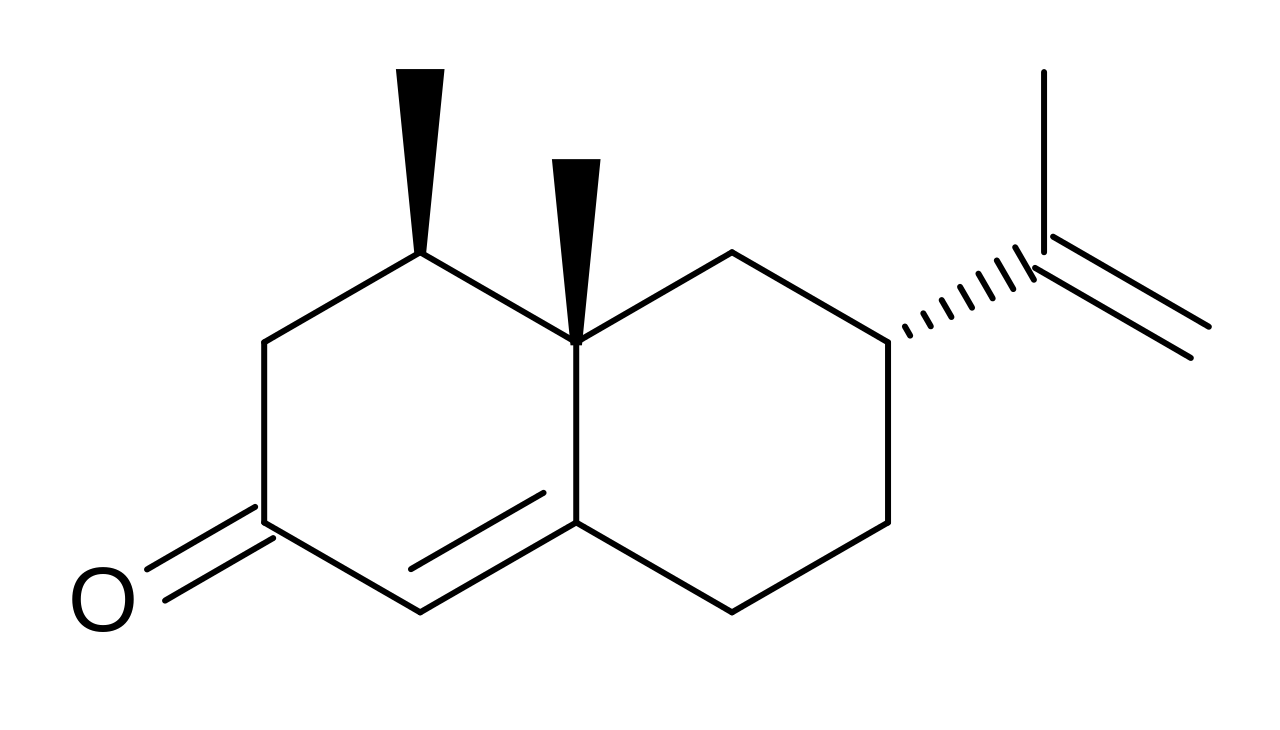
諾卡酮的天然來源
諾卡酮是從柚子皮油和阿拉斯加黃柏油中分離出的。這個物種的名字,nootkatensis,來源于加拿大nuu - cha - nulth人的語言(以前被稱為Nootka人)。
諾卡酮的基本性質及用途
無色或淡黃色油狀液體。純品熔點35~36℃,+185°~+186°。具持久而強的柑橘樣果香,在較低稀釋度時呈典型的柚子香氣。由具有相似立體結構骨架的巴侖西亞橘烯為原料氧化而得。主要用于配制各種柑橘型香精。
別名:圓柚酮,
其他名稱:5,6-二甲基-8-異丙烯基-二環-(4,4,0)-癸-1-烯-3-酮。分子式:C15H22O,相對分子質量:218.34。
理化性質:結晶體,不溶于水,溶于乙醇等有機溶劑,熔點36~37 ℃。
天然存在:柑桔、圓柚中。
香氣特征:具有圓柚、柑桔、橙子的氣味,并帶有甜的果皮、木香香韻。
應用:可用于調配圓柚、橙子、熱帶水果等食用香精和煙用香精。
在煙氣中的作用:具有增加卷煙香氣,豐滿卷煙香味和降低刺激的作用。
參考用量:在最終加香食品中的建議用量為10 mg/kg。
安全管理情況:FEMA編號為3166,FDA編號為 172.515,CoE編號為 11164,中國GB 2760-1996批準為暫時允許使用的食品香料。

諾卡酮廣泛應用于香精和香料行業
從瓦倫烯高效生產諾卡酮
最重要和最昂貴的葡萄柚香味,諾卡酮(2),可以降低體脂率,因此它的高效生產已被化妝品和食品工業部門迫切要求。[1]
此前,從巴倫西亞橙精油中提取的瓦倫烯(1)通過腸桿菌屬(Enterobacter sp.)轉化為諾卡酮(2)的轉化率僅為12%,紅球菌(Rodococcus KSM-5706)的轉化率為0.5%,和細胞色素P-450 (CYP450)的轉化率為20%。諾卡酮(2)由瓦倫烯(1)與AcOOCMe3和低產量鉻酸在三步法化學合成,使用表面官能化二氧化硅,由金屬催化劑,如Co2+和Mn2+與叔丁基過氧化氫可獲得75%的產。但這些合成方法并不安全,因為它們涉及有毒的重金屬。因此,設計一種不使用任何鉻、錳等重金屬的環境友好的諾卡酮合成方法迫在眉睫。從巴倫西亞橙油中得到的商業上可獲得的廉價倍半萜烴(+)-valencene(1)通過小球藻(Chlorella)、毛霉菌(Mucor)、葡萄座腔菌(Botryosphaeria dothidea)和可可球二孢菌(Botryodiplodia theobromae)的生物轉化可有效地合成諾卡酮(2)。[1]

圖1 小球藻對瓦倫烯(1)的生物轉化[1]
將淡色小球藻(Chlorella fusca var. vacuolata)IAMC-28接種于Noro培養基,光照固定培養。利用蔡貝克氏(czapek)-蛋白胨培養基對纖維素曲霉(Aspergillus cellulosae)、黑曲霉(A. niger)、葡萄座腔菌(B. dothidea)、可可球二孢菌(B. theobromae)、黃色鐮孢菌(Fusarium culmorum)和毛霉(Mucor)進行底物的生物轉化。Yoshiaki Noma實驗室從大阪府土壤中分離得到黑曲霉,并根據其生理形態特征進行鑒定。(+)-Valencene (1) (20 mg 50 ml)從巴倫西亞橙精油中分離出來,加入培養基中,由淡色小球藻(C. fusca)進一步轉化18天,產生諾卡酮(GC-MS峰面積:89%;分離的收率:63%)。由NaBH4和CeCl3還原2可以得到2α-羥基瓦倫烯(3),其得率為87%,然后與對硝基苯酸(p-nitrobenzoic acid),三苯基膦( triphenylphosphine),偶氮二甲酸二乙酯( diethyl azodicarboxylate)進行光延反應(Mitsunobu reaction),以合成從姜科植物益智(Alpinia oxyphylla)中分離得到具有鈣拮抗作用的諾卡酮(2β-羥基瓦倫烯)(4),其得率為42%。[1]
這樣得到的化合物3和4很容易被淡色小球藻(C. fusca)和蛋白核小球藻(C. pyrenoidosa)生物轉化,只需1天就能得到高產量(80-90%)的諾卡酮(2)。化合物1的生物轉化進一步由蛋白核小球藻(C. pyrenoidosa)和普通小球藻(C. vulgaris)以及土壤細菌進行,得到了較高的諾卡酮產量。在蛋白核小球藻(C. pyrenoidosa)對1進行生物轉化的時間過程中,在沒有2α-羥基瓦倫烯(3)的情況下,諾卡酮(2)和諾卡醇(4)的產量隨著化合物1產量的減少而增加,隨后2的產量隨著3產量的減少而增加。在瓦倫烯(1)的代謝途徑中,1緩慢轉化為諾卡醇(4),隨后4迅速轉化為2,如圖1所示。[1]
從土壤中分離出來的真菌菌株毛霉菌(Mucor sp.)被接種在蔡貝克氏(czapek)-蛋白胨培養基(pH7.0)中,在30℃下靜態培養7天,發現粘附在葉狀苔類蒼白球亞纖毛(Thalloid liverwort Pallavicinia subcilita)上。將化合物1(20毫克50毫升)加入培養基中,再培養7天。這導致了諾卡酮(2)的高產量(82%)。[1]
還使用從導致各種水果腐敗的真菌中分離出來的植物病原真菌葡萄座腔菌(B. dothidea)和可可球二孢菌(B. theobromae)(共31個菌株),對1到2的生物轉化進行了研究。同樣濃度的底物1與葡萄座腔菌(B. dothidea)和可可球二孢菌(B. theobromae)一起培養,得到諾卡酮(42-84%)。[1]
用于化妝品和食品工業的昂貴的柚子香味的諾卡酮(2)是通過(+)-瓦倫烯(valencene)(1)的生物轉化大量獲得的,這種香原料可以由小球藻、真菌如毛霉菌、葡萄座腔菌和可可球二孢菌從瓦倫西亞橙廉價獲得。這是一個非常廉價和清潔的氧化反應,不使用任何重金屬,因此這種方法有望在諾卡酮的工業生產中找到應用。[1]
諾卡酮的應用
噴霧形式的諾卡酮已被證明是對付鹿蜱和孤星蜱的有效驅蟲劑或殺蟲劑。它也是一種對付蚊子的有效驅蚊劑或殺蟲劑,還可以驅除臭蟲、頭虱和其他昆蟲它是一種環境友好型殺蟲劑,因為它是一種揮發性精油,在環境中不持久。美國環保局于2020年8月10日批準了它的這種用途。與香茅、薄荷油和檸檬草油等植物精油驅蚊劑相比,它驅蚊的能力可以持續幾個小時,它對人體無毒,是一種經批準的食品添加劑,通常用于食品、化妝品和藥品。

保護自己和家人免受蚊蟲和蜱蟲叮咬的最好方法是使用驅蟲劑

埃及伊蚊傳播的病毒包括登革熱、寨卡、奇昆古尼亞熱和黃熱病

黑腳蜱可以傳播多達7種病原體,包括導致萊姆病的細菌。
美國環保署(EPA)對諾卡酮的注冊為企業開發新型驅蟲劑鋪平了道路。
美國疾病控制與預防中心已經授權兩家公司生產一種殺蟲劑和一種驅蟲劑。加州圣地亞哥的Allylix公司(現為Evolva公司)是這些授權方之一,公司開發了一種酶發酵工藝,該工藝將比以前的工藝更經濟有效地生產諾卡酮。
1、諾卡酮:一種用于開發殺蟲劑和驅蟲劑的新活性成分[2]
諾卡酮,作為EPA注冊產品,允許制造商為消費者開發驅蟲劑,洗液和肥皂。諾卡酮是:一種在阿拉斯加黃杉樹和葡萄柚皮中發現的微量化合物。能夠擊退和殺死蜱蟲和昆蟲,包括蚊子。負責柚子特有的香味和口感。廣泛用于香精工業制造香水和古龍水。在皮膚和衣服上可以持續幾個小時。用于柑橘味的洗發水,護發素,洗液。廣泛應用于食品工業中,給食品調味。需要好幾噸葡萄柚才能產生1公斤(2.2磅)的諾卡酮。Evolva的工藝允許以高度可重復性和無污染的方式大量生產諾卡酮。曾經稀有而昂貴的諾卡酮現在的生產成本很低。[2]
諾卡酮是一種活性成分,而不是最終用途(品牌名稱)產品。有效成分使最終使用的產品有效。例如,避蚊胺(DEET)是許多品牌驅蟲劑中使用的活性成分。在EPA注冊后,CDC的獨家授權合作伙伴Evolva就可以將諾卡酮作為一種活性成分銷售給殺蟲劑和驅蟲劑;涂在皮膚上的驅蟲劑,公共衛生用途(非農業用途)的低量和超低量噴霧劑。[2]
諾卡酮有一種新穎的作用方式,諾卡酮似乎以一種獨特的方式殺死咬人的害蟲,不同于其他已經在EPA注冊的殺蟲劑。諾卡酮的作用不同于其他殺蟲劑,包括擬除蟲菊酯、有機磷、氨基甲酸酯和環二烯。用諾卡酮制成的殺蟲劑可以幫助消滅對現有蚊子產生抗藥性的蚊子。[2]
2、諾卡酮現已在美國環保署注冊[3]
由美國疾病控制與預防中心(CDC)發現和開發的一種新的活性成分已被美國環境保護署(EPA)注冊用于殺蟲劑和驅蟲劑。[3]
新的成分,諾卡酮,排斥和殺死蜱蟲,蚊子,和各種各樣的其他咬人的害蟲。諾卡酮負責葡萄柚特有的氣味和味道,被廣泛用于香水工業,制造香水和古龍水。在阿拉斯加的黃杉樹和葡萄柚皮中發現了微量的這種物質。[3]
諾卡酮現在可以用來開發新的驅蟲劑和殺蟲劑來保護人類和寵物。CDC的授權合作伙伴Evolva正在與領先的蟲害控制公司就可能的商業合作進行深入討論。有意開發品牌消費品的公司將被要求向美國環境保護署提交注冊包進行審查,這些產品最早將于2022年上市。[3]
“CDC很自豪能夠領導諾卡酮的研究和開發,”Jay C. Butler說,醫學博士,傳染病副主任。“為現有的預防咬傷方法提供新的替代方法,為解決預防病媒傳播疾病的最大挑戰之一——預防咬傷鋪平了道路。”[3]
研究表明,當諾卡酮被配制成驅蟲劑時,它們的保護效果可能與含有其他有效成分的產品相似,可以提供長達數小時的保護。[3]
諾卡酮以一種獨特的方式殺死咬人的害蟲,不同于其他已經在EPA注冊的殺蟲劑,包括擬除蟲菊酯、有機磷、氨基甲酸酯和環二烯。根據美國環保署的說法,擁有一種新的有效的殺蟲劑成分將有助于解決對目前使用的其他產品日益增長的殺蟲劑抗性水平。[3]
環保署化學品安全和污染預防辦公室助理署長亞歷山德拉·達波利托·鄧恩(Alexandra Dapolito Dunn)說:“環保署很高興繼續與疾病預防控制中心合作,注冊諾卡酮,這是幫助保護美國公眾免受昆蟲和扁虱叮咬的另一種工具。”“這種新的活性成分有潛力用于未來的驅蟲劑和殺蟲劑,保護人們免受疾病。在美國的許多地區,蚊子已經對現有的殺蟲劑產生了抗藥性。我們工具箱中的一種新的活性成分將有助于矢量控制項目。”[3]
蚊子和蜱蟲傳播的疾病在美國的每個州和地區都是一個日益嚴重的威脅。從2004年到2018年,報告的蚊媒傳播疾病病例數量翻了一番。在美國報告的所有病媒傳播疾病病例中,蜱媒傳播疾病占了近8 / 10。這些疾病風險的增加意味著對聯邦、州和地方衛生部門和病媒控制機構的要求越來越高。[3]
疾控中心從2014年開始與Evolva合作。2017年,Evolva獲得生物醫學高級研究和開發局(BARDA)合同,主要目標是推進諾卡酮和基于諾卡酮的產品的開發,以預防登革熱和寨卡病毒等蚊媒疾病。這項工作得到了美國疾病控制與預防中心聯邦基金的支持,并由負責防范和應對的助理國務卿辦公室(BARDA)根據第2號合同管理——HHSO100201700015C。[3]
諾卡酮的藥理或生物活性
1、非食品生物活性產品(+)-諾卡酮:化學和生物活性[4]
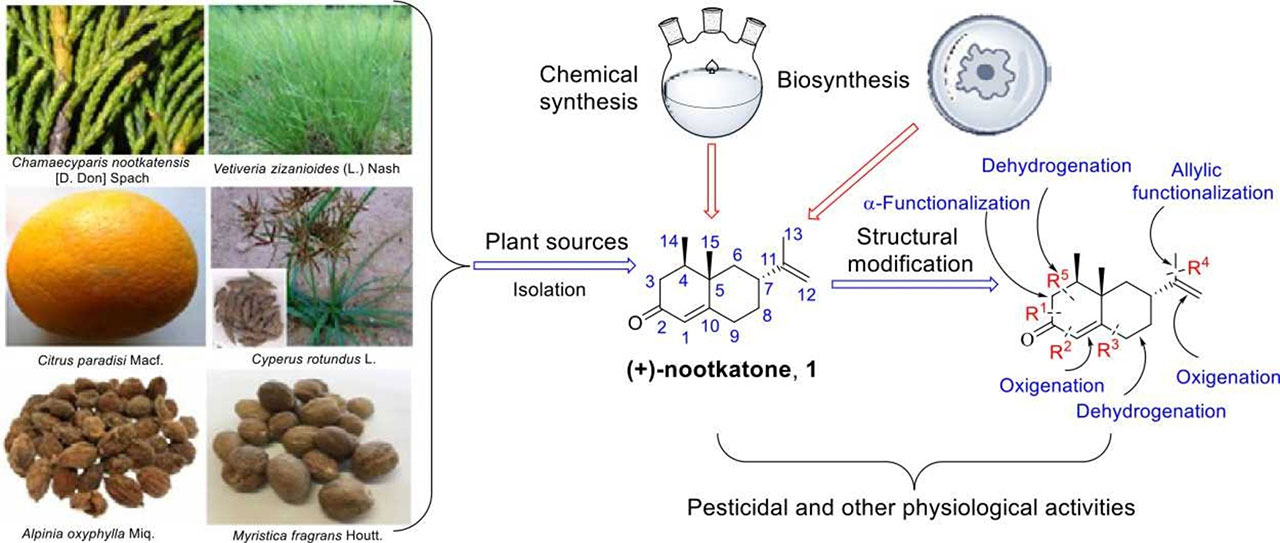
(+)-諾卡酮,首次從阿拉斯加黃杉(Chamaecyparis nootkatensis)的心材中分離出來,是一種非食用的天然倍半萜酮。由于其強烈的葡萄柚香味和廣泛的生物活性,(+)-諾卡酮在食品、化妝品、制藥和化工行業的需求日益增長。因此,需要結合現有的最新信息,了解(+)-諾卡酮的研究現狀,為(+)-諾卡酮及其類似物的進一步發展鋪平道路。本文綜述了(+)-諾卡酮的植物來源、化學合成、生物合成、結構修飾以及(+)-諾卡酮及其衍生物殺蟲活性和其他生理活性的研究進展。我們希望這項工作可以為(+)-諾卡酮及其類似物在食品、化妝品、制藥和化工行業的進一步應用提供參考。[4]
2、山姜屬益智仁(A. Oxyphylla)及其活性成分諾卡酮對結直腸癌細胞增殖的抑制作用
背景:山姜屬益智仁提取物具有廣泛的藥理活性。然而,益智仁及其活性化合物諾卡酮在結直腸癌中的分子機制尚不清楚。方法:我們的研究旨在研究益智仁及其生物活性化合物諾卡酮在體外抑制腫瘤中的作用。結果:益智仁提取物和諾卡酮對結直腸癌細胞均有抑制增殖作用。益智仁在結直腸癌細胞中表現出抗氧化活性,可能是通過誘導HO-1介導的。此外,在益智仁的存在下,促凋亡蛋白nag1和細胞增殖蛋白cyclin D1的表達分別升高和降低。當檢測抗腫瘤活性時,諾卡酮治療導致菌落和球狀形成的減少。相應地,諾卡酮也導致了nag1表達的增加和cyclin D1表達的減少。諾卡酮抑制cyclin D1的機制涉及蛋白水平調控,而諾卡酮在轉錄水平上增加nag1的表達。除了具有PPARγ結合活性,諾卡酮還能增加EGR-1的表達,最終導致nag1啟動子活性的增強。結論:綜上所述,諾卡酮是一種具有抗增殖和促凋亡活性的抗腫瘤化合物。[5]
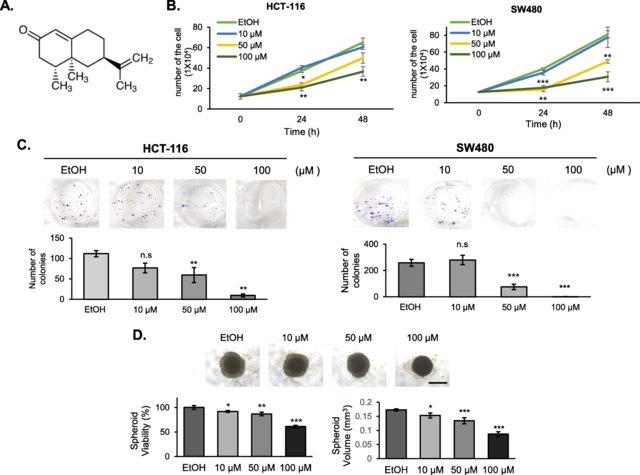
諾卡酮在結直腸癌細胞中顯示出抗癌活性。a諾卡酮的結構。b細胞增殖試驗。用不同濃度的諾卡酮處理HCT-116和SW480結直腸癌細胞,用血細胞計計數。y軸表示細胞號,x軸表示時間。以乙醇作為諾卡酮的載體。三個獨立實驗(n = 3)的量化結果以均數±SD表示,*p < 0.05、**p < 0.01、***p < 0.001表示有統計學意義。c菌落形成試驗。HCT-116和SW480細胞在含諾卡酮的培養基中生長9天。菌落數被計數并顯示在底部的圖表中。3個獨立實驗(n = 3)的結果均以均數±SD表示,*p < 0.05、**p < 0.01、***p < 0.001均有統計學意義。n,不重要。d橢球體活力測定。HCT-116腫瘤球形體用諾卡酮治療。相位對比圖像顯示,橢球體的大小,特別是增殖區大小呈劑量依賴性地縮小。比例尺代表500 μm。用CellTiter-Glo?3D細胞活力測定法(Promega)測定球形細胞活力。右圖,球體體積計算方法章節描述。該圖代表了三個獨立的實驗。*p < 0.05, **p < 0.01, ***p < 0.001[5]
3、諾卡酮抑制小鼠急性和慢性炎癥反應
諾卡酮(NTK)是一種倍半萜類化合物,存在于許多柑橘類植物(蕓香科)精油中。考慮到以往的報道表明NTK抑制炎癥信號通路,本研究旨在研究該化合物在小鼠急性和慢性炎癥模型中的作用。采用角叉菜膠、右旋糖酐、組胺、花生四烯酸所致小鼠足腫脹模型及角叉菜膠所致腹膜炎、胸膜炎觀察NTK對急性炎癥的影響。用棉球誘導的小鼠肉芽腫模型研究NTK治療對慢性炎癥的影響。在急性炎癥模型中,NTK表現出抗水腫作用和抑制白細胞募集,這與血管通透性降低、抑制髓過氧化物酶(MPO)、白細胞介素(IL)1-β和腫瘤壞死因子(TNF)-α的產生有關。在體分析表明,NTZ的抗炎作用也可能是由于抑制環氧化酶(COX)-2活性和拮抗組胺受體1 (H1)。在慢性炎癥模型中,這些機制可能有助于肉芽腫重量和勻漿蛋白濃度的降低。綜上所述,NTK的抗炎作用與抑制il - 1-β和TNF-α的產生有關,這可能與抑制COX-2活性和拮抗H1受體有關。然而,還需要進一步的研究來確定這種化合物對慢性炎癥的作用。[6]
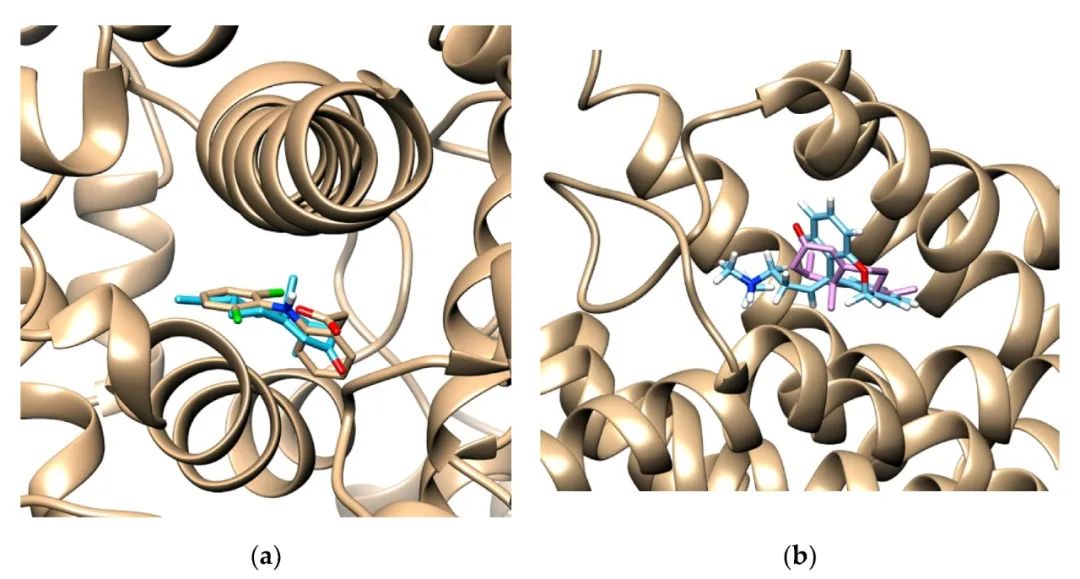
NTK和雙氯芬酸結合環氧合酶(COX)-2酶結合位點(a)和NTK和多塞平結合H1受體結合位點(b)的結合最穩定。
4、NQO1通過調節AMPK信號通路介導諾卡酮在脂多糖誘導的神經炎癥中的抗炎作用
神經炎癥和氧化應激在神經退行性疾病的進展中起關鍵作用。因此,使用有效的抗炎/抗氧化劑被認為是一種有前途的治療神經退行性疾病的策略。本實驗研究了從葡萄柚中分離的倍半萜化合物諾卡酮(nootkatone, NKT)在體外和體內神經炎癥模型中的抗炎和抗氧化作用。在脂多糖(LPS)刺激的BV2小膠質細胞中,NKT抑制iNOS、COX-2和促炎細胞因子的表達,并增加抗炎細胞因子IL-10的表達。此外,NKT抑制活性氧(ROS)的產生,上調抗氧化酶如NQO1和HO-1的表達。分子機制研究表明,NKT抑制lps刺激的BV2細胞中Akt、p38 MAPK和NF-κB的活性,同時增加AMPK、PKA/CREB和Nrf2/ARE信號通路。由于NKT顯著增加了NQO1的表達,我們通過藥物抑制或敲低實驗研究了這種酶的作用。使用NQO1特異性抑制劑雙香豆素或NQO1 siRNA處理BV2細胞可顯著阻斷nkt介導的NO、ROS、TNF-α、IL-1β和IL-10上調。此外,抑制NQO1逆轉了NKT對促炎和抗炎信號分子的作用。有趣的是,我們發現AMPK抑制劑化合物C模仿了雙香豆素的作用,表明NQO1和AMPK之間存在一種串聯。最后,我們發現NKT抑制lps注射小鼠大腦中的小膠質細胞激活、脂質過氧化和促炎標志物的表達,雙香豆素也能逆轉這一現象。這些數據表明,NQO1通過調節AMPK及其下游信號通路,在介導NKT在lps誘導的神經炎癥中的抗炎和抗氧化作用中發揮重要作用。[7]

NKT在lps刺激的小膠質細胞中具有抗炎和抗氧化作用。NKT抑制lps注射小鼠大腦中的小膠質細胞激活。NQO1介導NKT在體外和體內的抗炎/抗氧化作用。NQO1-AMPK信號在NKT抗炎機制中起關鍵作用。NKT在神經退行性疾病的治療中可能具有治療潛力。[7]
5、諾卡酮通過抑制氧化應激、炎癥和細胞凋亡,在肝纖維化小鼠模型中具有肝保護和抗纖維化作用
本研究以四氯化碳(CCl4)致小鼠肝纖維化為實驗材料,研究諾卡酮(NTK)的肝保護和抗纖維化作用。CCl4分別升高血清天門冬氨酸和丙氨酸轉氨酶水平。此外,CCl4產生肝臟氧化和硝態應激,其特征是血紅素氧合酶-1表達減少,抗氧化防御,4-羥基壬烯醛和3-硝基酪氨酸積累。此外,CCl4誘導肝組織中腫瘤壞死因子-α、單核細胞趨化蛋白-1、白細胞介素-1β等促炎因子的表達,與核因子κB激活密切相關。此外,CCl4處理的動物表現出更高的凋亡,其特征是caspase 3活性增加,DNA碎片化和多聚(adp -核糖)聚合酶激活。此外,組織學和生化檢查顯示CCl4給藥動物的肝臟明顯纖維化。然而,NTK處理減輕了CCl4誘導的表型變化。總之,我們的研究結果表明,NTK通過抑制氧化應激、炎癥和細胞凋亡發揮肝保護和抗纖維化作用。[8]

NTK對肝損傷及纖維化的影響。這顯示了各組動物血清中ALT (A)和AST (B)的水平。(C)肉眼檢查顯示CCl4給藥小鼠肝纖維化,經NTK減毒。n = 6 /組;#P < 0.0001 vs . Veh;*P < 0.01與CCl4;@P < 0.001 vs . CCl4。(D)分別處理組制備的石蠟包埋肝臟切片具有代表性的蘇木精和伊紅(H&E)染色。CCl4誘導大結節、纖維間隔、脂肪變性、肝細胞自吸和壞死、炎癥細胞浸潤。然而,NTK治療消除了ccl4誘導的肝組織損傷,并保留了組織結構。最后200×放大;比例尺= 50?m. [8]
參考文獻:
[1] Yoshinori Asakawa, Yoshiaki Noma,3.20 - Biotransformation of Sesquiterpenoids,Editor(s): Hung-Wen (Ben) Liu, Lew Mander, Comprehensive Natural Products II,Elsevier,2010,Pages 803-892,
ISBN 9780080453828,https://doi.org/10.1016/B978-008045382-8.00066-6.
[2] https://www.cdc.gov/ncezid/dvbd/media/dpk-nootkatone.html
[3] https://www.cdc.gov/media/releases/2020/p0810-nootkatone-registered-epa.html
[4] Jiangping Fan, Zhiyan Liu, Shengnan Xu, Xiaoting Yan, Wanqing Cheng, Ruige Yang, Yong Guo,Non-food bioactive product (+)-nootkatone: Chemistry and biological activities,Industrial Crops and Products,Volume 177,2022,114490,https://doi.org/10.1016/j.indcrop.2021.114490.
[5] Yoo, Eunsu & Lee, Jaehak & Lertpatipanpong, Pattawika & Ryu, Junsun & Kim, Chong-Tai & Park, Eul-Yong & Baek, Seung. (2020). Anti-proliferative activity of A. Oxyphylla and its bioactive constituent nootkatone in colorectal cancer cells. BMC cancer. 20. 881. 10.1186/s12885-020-07379-y.
[6]Bezerra Rodrigues Dantas L, Silva ALM, da Silva Júnior CP, Alcantara IS, Correia de Oliveira MR, Oliveira Brito Pereira Bezerra Martins A, Ribeiro-Filho J, Coutinho HDM, Rocha Santos Passos F, Quintans-Junior LJ, Alencar de Menezes IR, Pezzani R, Vitalini S. Nootkatone Inhibits Acute and Chronic Inflammatory Responses in Mice. Molecules. 2020; 25(9):2181. https://doi.org/10.3390/molecules25092181
[7] Jung-Eun Park, Jin-Sun Park, Yea-Hyun Leem, Do-Yeon Kim, Hee-Sun Kim,NQO1 mediates the anti-inflammatory effects of nootkatone in lipopolysaccharide-induced neuroinflammation by modulating the AMPK signaling pathway,Free Radical Biology and Medicine,164,2021,354-368 doi. 10.1016/j.freeradbio med.2021.01.015.
[8] Kurdi, Amani; Hassan, Kamal; Venkataraman, Balaji; Rajesh, Mohanraj (2017). Nootkatone confers hepatoprotective and anti-fibrotic actions in a murine model of liver fibrosis by suppressing oxidative stress, inflammation, and apoptosis. Journal of Biochemical and Molecular Toxicology, e22017. doi: 10. 1002 / jbt. 22017.